Kalijum karbonat
Appearance
| |
| |

| |
| Nazivi | |
|---|---|
| IUPAC naziv
Kalijum karbonat
| |
| Drugi nazivi
Potaša
| |
| Identifikacija | |
| ECHA InfoCard | 100.008.665 |
| Е-бројеви | E501(i) (регулатор киселости, ...) |
| MeSH | Potassium+carbonate |
| RTECS | TS7750000 |
| Svojstva | |
| K2CO3 | |
| Molarna masa | 138,2055 g/mol |
| Agregatno stanje | Čvrsta bela higroskopna supstanca |
| Gustina | 2,29 g/cm³, основно |
| Tačka topljenja | 891 °C |
| Tačka ključanja | razgrađuje se |
| 112 g/100 mL (20 °C) | |
| Opasnosti | |
| NFPA 704 | |
| Tačka paljenja | nije zapaljiv |
| Srodna jedinjenja | |
Drugi katjoni
|
litijum-karbonat, natrijum-karbonat, cezijum-karbonat |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |
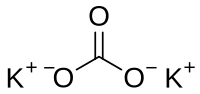
Kalijum karbonat (molekulska formula K2CO3) je hemijsko jedinjenje, kalijumova so ugljene kiseline.[1][2] Kalijum karbonat je bezbojna kristalna supstancija veoma dobro rastvorljiva u vodi; 93.7 g u 100 g vode. Temperatura topljenja kalijum karbonata iznosi 891°C. On gradi hidrate, u vodenim rastvorima se hidrolizuje. Pod uticajem kiselina podleže raspadu na ugljen-dioksid i kalijum oksid.
Kalijum karbonat se dobija uvođenjem ugljen-dioksida u vodeni rastvor kalijum hidroksida. Koristi se u industriji stakla, keramike, za produkciju sredstava za pranje, u fotografiji i za dobijanje drugih jedinjenja kalijuma.
Molekulska masa kalijum karbonata je 138.2 u.
Vidi još
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. izd.). Prentice Hall. ISBN 978-0-13-175553-6.
- ^ Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st izd.). San Diego: Academic Press. ISBN 0-12-352651-5.

