Паулијев принцип
Паулијев принцип искључења је принцип у квантној механици, који је 1925. формулисао Волфганг Паули. Гласи да ниједна два идентична фермиона не могу да се налазе у истом квантном стању симултано. Ригорозније тврђење овог принципа је да је, за два идентична фермиона, укупна таласна функција антисиметрична. За електроне у једном атому, гласи да ниједна два електрона не могу да имају иста четири квантна броја, то јест ако су n, l, и ml једнаки, ms мора бити различит тако да електрони имају супротне спинове. Ово је кључни принцип за разумевање и изградњу Периодног система елемената. Волфганг Паули, је за формулисање овог принципа 1945. добио Нобелову награду за физику.



Паулијев принцип искључења објашњава електронска конфигурација, то јест смештај електрона у љускама атомског омотача, а тиме и периодичност својстава хемијских елемената. Њему се подвргавају и електрони у електронском плину у металима, на чему почива теорија електричне проvoдљивости, а објашњава и многа механичка, електрична, магнетска, оптичка и хемијска својства чврстих материја. Паули је то начело објаснио (формулирао) 1925. за електроне, а 1940. га је проширио од електрона на све фермионе, честице с полуцелим спином. У општем објашњењу, Паулијево начело изриче да таласна функција мора бити антисиметрична при замени двају фермиона, односно симетрична при замени пара бозона. То се начело показује важним за стабилност атома и хемијских материја генерално.[1]
Једна од последица принципа искључења јесте чињеница да постоје разни хемијски елементи, јер када он не би вредео, тада би сви електрони у атому заузели најниже енергетско стање, те би по хемијским својствима били једнаки. Електрони атома тежих од хелијумових не заузимају најниже енергетско стање, јер два електрона у истом атому не могу имати сва четири квантна броја (n, l, ml и ms) једнака, што значи да не могу бити описана једнаком таласном функцијом.
Ауфбау принцип
[уреди | уреди извор]Ауфбау принцип или принцип изградње је принцип попуњавања орбитала у вишеелектронским атомима који се првенствено ослања на Паулијев принцип, тј. на услов да два електрона у истој љусци морају имати барем један различит квантни број. Код Ауфбау принципа када се попуњавају електронске љуске и када се не разматра се спин, кватни бројеви вишеелектронских атома су: n, l, и λ. Попуњене електронске љуске неће имати спин, ни орбитални момент импулса.[2]
Квантни бројеви и Паулијево начело
[уреди | уреди извор]Да би се добила груба слику атома, може се занемарити силе између електрона. Тад се сваки електрон креће око атомског језгра у стазама. Ова груба слика атома омогућава да се нађу квантни бројеви и стационарна стања електрона, који се добијају и у прецизнијим моделима атома.
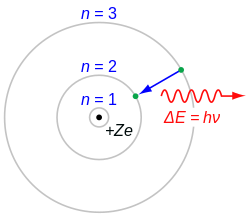
Из рендгенских спектара се види да главни квантни број н, којим су дате водоникове енергије, одређује поједине љуске атома. У Боровом моделу водоника главни квантни број одређује велику полуосу елиптичне стазе електрона. Према том главном квантном броју обележавају се поједине љуске:
| n = | 1 | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|---|
| љуска | K | L | M | N | O | P |
n = 1 одговара стабилном стању, n = 2 првом побуђеном нивоу и тако даље. Према томе, K љуска представља енергетски најнижу, најстабилнију љуску, L љуска прву изнад најниже, и тако даље.
У Боровом моделу више елипса припада главном квантном броју. Изузетак чини најнижа љуска n = 1, којој одговара само једна кружница. Колики је главни квантни број n, толико има различитих елипса. Оне одговарају различитим дискретним вредностима импулса вртње. Другој љуски одговарају у Борову моделу два различита импулса вртње са nφ = 1, nφ = 2 и nφ = 3.
Битну промену на Боров модел је извршила строга квантна механика (В. Хајзенберг, Е. Шредингер). Према строгој квантној механици импулс вртње електрона око језгра може бити једнак нули. То је управо оно што је код водоника искључено. Било је речено да би тад електрони титрали у правцу и пролазили кроз језгро. Међутим, за строгу квантну механику не постоје такве тешкоће, јер се она у самом почетку одрекла наивних визуелних слика. Искуство је дало право модерној квантној теорији. По Бору би се електрон у стабилном стању водониковог атома морао вртети у кружници и имати импулс вртње h/2∙π. Штерн и Герлах су успели да тачно измере импулс вртње и магнетни момент водониковог атома. Пролазећи кроз нехомогено магнетско поље, водоникови се зраци цепају у два снопа. Овај дволом одговара моменту импулса 1/2∙h/2∙π. Једини импулс вртње, што га има водиков атом у стабилном стању, потиче од спина. И за друге атоме доказано је то исто. Импулси вртње могу, дакле, попримити и вредност нула.
Уместо старог квантног броја nφ уведен је нови квантни број вртње l, тако да он поприма редом вредности 0, 1, 2, 3, … Највећа вредност, коју тај квантни број у појединој љуски може имати, износи n - 1. Добија се опет, као и у старој квантној теорији, за сваку љуску n различитих вртња. Код K љуске је l = 0, код L љуске l = 0 и l = 1, код M љуске је l = 0, l = 1 и l = 2. Оvo се наставља на следећи начин:
| n = 1 | n = 2 | n = 3 | n = 4 | n = 5 |
|---|---|---|---|---|
| l = 0 | l = 0 | l = 0 | l = 0 | l = 0 |
| l = 1 | l = 1 | l = 1 | l = 1 | |
| l = 2 | l = 2 | l = 2 | ||
| l = 3 | l = 3 | |||
| l = 4 |
Тиме су исцрпљени сви типови стаза. Међутим, како је познато, раван кретања електрона око језгра може још имати различите положаје у простору. Из Зеемановог учинка и Стерн-Герлахових експеримената закључено је да су могуће оне оријентације момента импулса код којих су пројекције на задани смер једнаке m∙h/2∙π. Магнетски квантни број m поприма све целе бројеве од - л до + л. Могуће вредности магнетског квантног броја m забележене су у табели:
| l = 0 | 0 | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| l = 1 | - 1 | 0 | + 1 | ||||||
| l = 2 | - 2 | - 1 | 0 | + 1 | + 2 | ||||
| l = 3 | - 3 | - 2 | - 1 | 0 | + 1 | + 2 | + 3 | ||
| l = 4 | - 4 | - 3 | - 2 | - 1 | 0 | + 1 | + 2 | + 3 | + 4 |
Квантном броју l припада 2∙l + 1 различитих вредности магнетског квантног броја.
У Бор-Сомерфелдовој теорији 3 квантна бројa n, l и m одређују стазу електрона, и облик елипсе и њен нагиб према одређеном смеру. Исте те квантне бројеве преузела је и строга квантна механика, само што су они изгубили оно визуелно значење које им је приписивала стара теорија.
Још нисмо потпуно одредили стање електрона. Треба да узмемо у обзир и властиту вртњу електрона (спин). Како смо видели из Стерн-Герлахових експеримената, могуће су само две оријентације спина према магнетском пољу: паралелна и антипаралелна. Према томе уведен је квантни број спина s, који може попримити само две вредности:
- s = - 1/2 i s = + 1/2
Паралелном смеру одговара момент импулса + 1/2∙h/2∙π, а антипаралелном - 1/2∙h/2∙π. Других вредности спин нема.
Квантни бројеви n, l, m и s тачно одређују поједино стационарно стање електрона у атому водоника. Чим се одаберу 4 вредности квантних бројева, утврди се тачно кретање електрона.
Квантни бројеви n, l, m и s тачно одређују поједино стационарно стање и за друге елементе, уколико се занемаре силе између електрона. Тад се опет електрони крећу у елипсама око атомског језгра, само што је сад набој језгра једнак Ze. Ако се жели да се од те слике атома учини корак даље, морају се узети у обзир и силе између електрона. Међутим, сада се могу употребити стари квантни бројеви. Узајамне силе електрона модификујају кретање електрона, али оне не разарају стара стационарна стања и не стварају нова. Кад се узму у обзир међусобне силе електрона, тад се, у првом реду мењају енергије самих првобитних стационарних стања. Стационарна стања исте љуске немају више једнаку енергију. Како што је већ показано, енергија се то јаче снижава што је квантни број l мањи (стазе продиру у унутрашње љуске!). Сваки водоников енергетски ниво распада се на групу уско приљубљених нивоа. Али сам број стационарних стања остаје исти, а то је управо најважније за теорију периодног система.
Средишње је питање теорије како су смештени електрони на поједина стационарна стања. Чињенице о рендгенским спектрима показале су, да се никако не може претпоставити да се сви електрони налазе у најнижем стационарном стању. Код тешких атома налазе се електрони у L, M и N љуски. Нека сила спречава да ти електрони падну на најнижу љуску, што би значило стање најниже енергије, дакле највеће стабилности.
Кључ по којему су електрони распоређени на различита стационарна стања пружа такозвано Паулијево начело искључења. То начело је од темељног значења за теорију хемијских елемената и њихових спектара. По том начелу може исто квантно стање запосести само један електрон. Искључено је да у атому два електрона имају исте квантне бројеве n, l, m и s.
Паулијево начело доказано је низом спектроскопских експеримената. Оно је водич кроз сложени периодни систем елемената.[3]
Референце
[уреди | уреди извор]- ^ Paulijevo načelo (Paulijev princip), [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2019.
- ^ Белић, Драгољуб (2000). Физика молекула. Београд. стр. 106—109.
- ^ Ivan Supek: "Nova fizika", Školska knjiga Zagreb, 1966.
Литература
[уреди | уреди извор]- С. Мацура, Ј. Радић-Перић, АТОМИСТИКА, Факултет за физичку хемију Универзитета у Београду/Службени лист, Београд, 2004, стр. 438.
- Dill, Dan (2006). „Chapter 3.5, Many-electron atoms: Fermi holes and Fermi heaps”. Notes on General Chemistry (2nd ed.). W. H. Freeman. ISBN 978-1-4292-0068-4.
- Liboff, Richard L. (2002). Introductory Quantum Mechanics. Addison-Wesley. ISBN 978-0-8053-8714-8.
- Massimi, Michela (2005). Pauli's Exclusion Principle. Cambridge University Press. ISBN 978-0-521-83911-2.
- Tipler, Paul; Llewellyn, Ralph (2002). Modern Physics (4th ed.). W. H. Freeman. ISBN 978-0-7167-4345-3.
- Scerri, Eric (2007). The periodic table: Its story and its significance
 . New York: Oxford University Press. ISBN 9780195305739.
. New York: Oxford University Press. ISBN 9780195305739. - Dirac, Paul A. M. (1982). Principles of quantum mechanics. Oxford University Press. ISBN 0-19-852011-5.
- Griffiths, David J. (2004). Introduction to Quantum Mechanics (2nd ed.)
 . Prentice Hall. ISBN 0-13-805326-X.
. Prentice Hall. ISBN 0-13-805326-X. - Halzen, Francis; Martin, Alan D. (1984). QUARKS AND LEPTONS: An Introductory Course in Modern Particle Physics
 . John Wiley & Sons. ISBN 0-471-88741-2.
. John Wiley & Sons. ISBN 0-471-88741-2. - Chester, Marvin (1987). Primer of Quantum Mechanics. ISBN 0-486-42878-8.. John Wiley.
- Cox, Brian; Forshaw, Jeff (2011). The Quantum Universe: Everything That Can Happen Does Happen. Allen Lane. ISBN 978-1-84614-432-5.
- Richard Feynman (1985). QED: The Strange Theory of Light and Matter. Princeton University Press. ISBN 0-691-08388-6. Four elementary lectures on quantum electrodynamics and quantum field theory, yet containing many insights for the expert.
- Ghirardi, GianCarlo, 2004. Sneaking a Look at God's Cards, Gerald Malsbary, trans. Princeton University Press. The most technical of the works cited here. Passages using algebra, trigonometry, and bra–ket notation can be passed over on a first reading.
- N. David Mermin, , "Spooky actions at a distance: mysteries of the QT" in his. Boojums all the way through. Cambridge University Press. 1990.: 110–76.
- Victor Stenger, (2000). Timeless Reality: Symmetry, Simplicity, and Multiple Universes. Buffalo NY: Prometheus Books.. Chpts. 5–8. Includes cosmological and philosophical considerations.
More technical:
- Bernstein, Jeremy (2009). Quantum Leaps. Cambridge, Massachusetts: Belknap Press of Harvard University Press. ISBN 978-0-674-03541-6.
- Bohm, David (1989). Quantum Theory
 . Dover Publications. ISBN 978-0-486-65969-5.
. Dover Publications. ISBN 978-0-486-65969-5. - Eisberg, Robert; Resnick, Robert (1985). Quantum Physics of Atoms, Molecules, Solids, Nuclei, and Particles (2nd изд.). Wiley. ISBN 978-0-471-87373-0.
- Bryce DeWitt, R. Neill Graham, eds.,. (1973). The Many-Worlds Interpretation of Quantum Mechanics. ISBN 0-691-08131-X., Princeton Series in Physics, Princeton University Press.
- Everett, Hugh (1957). „Relative State Formulation of Quantum Mechanics”. Reviews of Modern Physics. 29 (3): 454—462. Bibcode:1957RvMP...29..454E. S2CID 17178479. doi:10.1103/RevModPhys.29.454.
- Feynman, Richard P.; Leighton, Robert B.; Sands, Matthew (1965). The Feynman Lectures on Physics. 1—3. Addison-Wesley. ISBN 978-0-7382-0008-8.
- D. Greenberger, K. Hentschel, F. Weinert, eds., 2009. Compendium of quantum physics, Concepts, experiments, history and philosophy, Springer-Verlag, Berlin, Heidelberg.
- Max Jammer, 1966. The Conceptual Development of Quantum Mechanics. McGraw Hill.
- Hagen Kleinert, 2004. Path Integrals in Quantum Mechanics, Statistics, Polymer Physics, and Financial Markets, 3rd ed. Singapore: World Scientific. Draft of 4th edition.
- L.D. Landau, E.M. Lifshitz (1977). Quantum Mechanics: Non-Relativistic Theory. 3 (3rd изд.). Pergamon Press. ISBN 978-0-08-020940-1. Online copy
- Gunther Ludwig,. (1968). Wave Mechanics. London: Pergamon Press. ISBN 0-08-203204-1.
- George Mackey (2004). The mathematical foundations of quantum mechanics. ISBN 0-486-43517-2.. Dover Publications. .
- Merzbacher, Eugen (1998). Quantum Mechanics. Wiley, John & Sons, Inc. ISBN 978-0-471-88702-7.
- Albert Messiah, 1966. Quantum Mechanics (Vol. I), English translation from French by G.M. Temmer. North Holland, John Wiley & Sons. Cf. chpt. IV, section III. online
- Omnès, Roland (1999). Understanding Quantum Mechanics. Princeton University Press. ISBN 978-0-691-00435-8. OCLC 39849482.
- Stone, A. Douglas (2013). Einstein and the Quantum
 . Princeton University Press. ISBN 978-0-691-13968-5.
. Princeton University Press. ISBN 978-0-691-13968-5. - Transnational College of Lex (1996). What is Quantum Mechanics? A Physics Adventure. Language Research Foundation, Boston. ISBN 978-0-9643504-1-0. OCLC 34661512.
- Veltman, Martinus J.G. (2003), Facts and Mysteries in Elementary Particle Physics.
Спољашње везе
[уреди | уреди извор]- Nobel Lecture: Exclusion Principle and Quantum Mechanics Pauli's account of the development of the Exclusion Principle.
