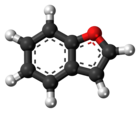
Бензофуран
Изглед
| |||
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
1-Benzofuran
| |||
| Други називи
Кумарон, бензо[б]фуран
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.439 | ||
| КЕГГ[1] | |||
| УНИИ | |||
| |||
| Својства | |||
| C8H6O | |||
| Моларна маса | 118,14 g·mol−1 | ||
| Тачка топљења | −18 °C (0 °F; 255 K) | ||
| Тачка кључања | 173 °C (343 °F; 446 K) | ||
| Опасности | |||
| Летална доза или концентрација (ЛД, ЛЦ): | |||
ЛД50 (ЛД50)
|
500 мг/кг (мице).[4] | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
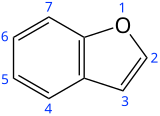
Бензофуран је хетероциклично једињење који се састоји од кондензованих прстена бензена и фурана. Ова безбојна течност је компонента катрана. Бензофуран је основа многих сродних једињења са комплекснијим структурама. На пример, псорален је дериват бензофурана који се јавља у неколико биљки.
Продукција
[уреди | уреди извор]Бензофуран се може екстраховати из катрана. Он се такође добија дехидрогенацијом 2-етилфенола.[4]
Лабораторијски методи
[уреди | уреди извор]Бензофуран се може припремити путем О-алкилације салицилалдехида са хлоросирћетном киселином и накнадном дехидратацијом насталог етра.[5] У другом методу званом Перкиново преуређење[6][7][8] кумарин реагује са хидроксидом:
Сродна једињења
[уреди | уреди извор]Референце
[уреди | уреди извор]- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б Collin, G.; Höke, H. (2007). „Benzofurans”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.l03_l01.
- ^ Burgstahler, A. W.; Worden, L. R. (1966). „Coumarone” (PDF). Org. Synth. 46: 28.; Coll. Vol., 5, стр. 251
- ^ Perkin, W. H. (1870). „XXIX. On some New Bromine Derivatives of Coumarin”. Journal of the Chemical Society. 23: 368—371. doi:10.1039/JS8702300368.
- ^ Perkin, W. H. (1871). „IV. On some New Derivatives of Coumarin”. Journal of the Chemical Society. 24: 37—55. doi:10.1039/JS8712400037.
- ^ Bowden, K.; Battah, S. (1998). „Reactions of Carbonyl Compounds in Basic Solutions. Part 32. The Perkin Rearrangement”. Journal of the Chemical Society, Perkin Transactions 2. 1998 (7): 1603—1606. doi:10.1039/a801538d.