Метаболизам гвожђа код човека
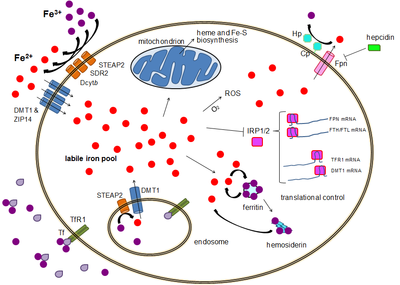
Метаболизам гвожђа код човека је сет хемијских реакција које одржавају људску хомеостазу гвожђа на системском и ћелијском нивоу. Гвожђе је неопходно телу, али је исто тако потенцијално токсично, и контролисање нивоа гвожђа у телу је од критичне важности за многе аспекте људског здравља и спречавање болести. Хематолози имају посебан интерест у системски метаболизам гвожђа јер је оно есенцијално за црвена крвна зрнца, у којима је највећи део гвожђа у људском телу садржан. Разумевање метаболизма гвожђа је исто тако важно за разумевање болести услед презасићености гвожђем, као што је наследна хемохроматоза, и дефицијенције гвожђа, као што је анемија дефицијенције гвожђа.
Значај регулације гвожђа
[уреди | уреди извор]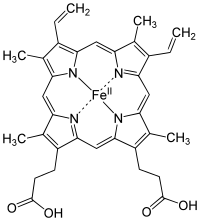
Гвожђе је есенцијални биоелемент за већину форми живота, од бактерија до сисара. Његов значај лежи у његовој способности да посредује трансфер електрона. У свом феро стању, гвожђе делује као донор електрона, док у фери стању делује као акцептор. Стога, гвожђе има виталну улогу у катализи ензиматских реакција у којима долази до електронског трансфера (редукцији и оксидацији, редокс). Протеини могу да садрже гвожђе као део различитих кофактора, као што су гвожђе сумпорни кластери (Fe-S) и хем групе, који се формирају у митохондријама.
Ћелијска респирација
[уреди | уреди извор]Људским ћелијама је неопходно гвожђе да би могле да добијају енергију у виду АТП молекула у вишестепном процесу познатом као ћелијска респирација, специфичније из оксидативне фосфорилације у митохондријским кристама. Гвожђе је присутно у гвоздено-сумпорним клустерима и хем групама у протеинима ланца транспорта електрона који генеришу протонски градијент чиме се омогућава АТП синтази да синтетише АТП (хемиосмоза).
Хем групе су део хемоглобина, протеина присутног у црвеним крвним зрнцима који учествује у транспорту кисеоника од плућа до ткива. Хем групе су исто тако присутне у миоглобину којим се складиђти и дифузно преноси кисеоник у мишићним ћелијама.
Кисеоникчни транспорт
[уреди | уреди извор]Људском телу је неопходно гвожђе за транспорт кисеоника. Кисеоник (О2) је потребан ради функционисања и опстанка скоро свих ћелијских типова. Кисеоник се транспортује из плућа до остатка тела везан за хем групу хемоглобина у еритроцитима. У мишићним ћелијама, гвожђе је везано у миоглобину, који регулише његово ослобађање.
Токсичност
[уреди | уреди извор]Гвожђе је исто тако потенцијално токсично. Његова способност да донира и прима електроне значи да оно може да катализује конверзију водоник пероксида у слободне радикале. Слободни радикали могу да направе штету у разним ћелијским структура, и ултиматно да доведу до смрти ћелије.[1]
Гвожђе везано за протеине или кофакторе као што је хем је безбедно. Такође, виртуално не постоје потпуно слободни јони гвожђа у ћелији, пошто они с лакоћом формирају комплексе са органским молекулима. Међутим, део интраћелијских јона је везан у нискоафинитетним комплексима, и назива се лабилним гвожђем или „слободним” гвожем. Гвожђе у таквим комплексима може да урокује штету као што је горе описано.[2]
Да би се спречила таква врста штете, све животне форме које користе гвожђе везују атоме гвожђа за протеине. Ово везивање омогућава ћелијама да користе гвожђе уз истовремено ограничавање његове способности да наноси повреде.[1][3] Типично су интраћелијске концентрације лабилног гвожђа код бактерија на нивоу од 10-20 микромола,[4] мада оне могу да буду десет пута веће у анаеробном окружењу,[5] где су слободни радикали и реактивне кисеоничне врсте ређе. У ћелијама сисара, концентрације интраћелијског лабилног гвожђа су типично мање од 1 микромола, што је мање од 5 процената укупног ћелијског гвожђа.[2]
Референце
[уреди | уреди извор]- ^ а б Цонрад МЕ, Умбреит ЈН (април 2000). „Дисордерс оф ирон метаболисм”. Тхе Неw Енгланд Јоурнал оф Медицине. 342 (17): 1293—4. ПМИД 10787338. дои:10.1056/НЕЈМ200004273421716.
- ^ а б Какхлон О, Цабантцхик ЗИ (2002). „Тхе лабиле ирон поол: цхарацтеризатион, меасуремент, анд партиципатион ин целлулар процессес”. Фрее Радицал Биологy анд Медицине. 33 (8): 1037—1046. дои:10.1016/с0891-5849(02)01006-7.
- ^ Андреwс НЦ (децембар 1999). „Дисордерс оф ирон метаболисм”. Тхе Неw Енгланд Јоурнал оф Медицине. 341 (26): 1986—95. ПМИД 10607817. дои:10.1056/НЕЈМ199912233412607.
- ^ Yан Y, Wаите-Цусиц ЈГ, Куппусамy П, Yоусеф АЕ (јануар 2013). „Интрацеллулар фрее ирон анд итс потентиал роле ин ултрахигх-прессуре-индуцед инацтиватион оф Есцхерицхиа цоли”. Апплиед анд Енвиронментал Мицробиологy. 79 (2): 722—724. ПМЦ 3553779
 . ПМИД 23124235. дои:10.1128/аем.02202-12.
. ПМИД 23124235. дои:10.1128/аем.02202-12.
- ^ Yамамото Y, Фукуи К, Коујин Н, Охyа Х, Кимура К, Камио Y (2004). „Регулатион оф тхе интрацеллулар фрее ирон поол бy Дпр провидес оxyген толеранце то Стрептоцоццус мутанс.”. Јоурнал оф Бацтериологy. 186 (18): 5997—6002. ПМЦ 515136
 . ПМИД 15342568. дои:10.1128/јб.186.18.5997-6002.2004.
. ПМИД 15342568. дои:10.1128/јб.186.18.5997-6002.2004.
Литература
[уреди | уреди извор]- Андреwс С, Нортон I, Салункхе АС, Гоодлуцк Х, Алy WС, Моурад-Агха Х, Цорнелис П (2013). „Цхаптер 7, Цонтрол оф Ирон Метаболисм ин Бацтериа”. Ур.: Банци L. Металломицс анд тхе Целл. Метал Ионс ин Лифе Сциенцес. 12. Спрингер. ИСБН 978-94-007-5560-4. дои:10.1007/978-94-007-5561-1_7. елецтрониц-боок ISBN 978-94-007-5561-1 ИССН 1559-0836 елецтрониц{иссн|1868-0402}
- Андреwс НЦ (мај 2004). „Анемиа оф инфламматион: тхе цyтокине-хепцидин линк”. Тхе Јоурнал оф Цлиницал Инвестигатион. 113 (9): 1251—3. ПМЦ 398435
 . ПМИД 15124013. дои:10.1172/ЈЦИ21441.
. ПМИД 15124013. дои:10.1172/ЈЦИ21441. - Цамасцхелла C (децембар 2005). „Ундерстандинг ирон хомеостасис тхроугх генетиц аналyсис оф хемоцхроматосис анд релатед дисордерс”. Блоод. 106 (12): 3710—7. ПМИД 16030190. дои:10.1182/блоод-2005-05-1857.
- Фразер ДМ, Андерсон ГЈ (октобар 2005). „Ирон импортс. I. Интестинал ирон абсорптион анд итс регулатион”. Америцан Јоурнал оф Пхyсиологy. Гастроинтестинал анд Ливер Пхyсиологy. 289 (4): Г631—5. ПМИД 16160078. дои:10.1152/ајпги.00220.2005.
- Инсел П, Росс D, МцМахон К, Бернстеин M (2011). „Ирон”. Нутритион (4тх изд.). Судбурy, Массацхусеттс: Јонес анд Бартлетт Публисхерс. стр. 510—514. ИСБН 978-0-7637-7663-3. Приступљено 25. 6. 2012. Сее еспп. 513-514
- Ламми-Кееф ЦЈ, Цоуцх СЦ, Пхилипсон ЕХ, ур. (2008). „Диетарy диверсифицатион анд модифицатион оф ирон”. Хандбоок оф Нутритион анд Прегнанцy. Нутритион & Хеалтх. Тотоwа, Неw Јерсеy: Хумана Пресс. стр. 350—351. ИСБН 978-1-59745-112-3. дои:10.1007/978-1-59745-112-3. Приступљено 25. 6. 2012.
- Мицронутриентс, Панел он; Субцоммиттеес он Уппер Референце Левелс оф Нутриентс анд оф Интерпретатион анд Усес оф Диетарy Референце Интакес; тхе Стандинг Цоммиттее он тхе Сциентифиц Евалуатион оф Диетарy Референце Интакес (2001). „Ирон”. Диетарy Референце Интакес фор Витамин А, Витамин К, Арсениц, Борон, Цхромиум, Цоппер, Иодине, Ирон, Манганесе, Молyбденум, Ницкел, Силицон, Ванадиум, анд Зинц. Wасхингтон, D.C: Фоод анд Нутритион Боард, Институте оф Медицине. стр. 290—393. ИСБН 978-0-309-07279-3. Приступљено 25. 6. 2012.
- Реиллy, C. (2004). „Ирон”. Тхе Нутритионал Траце Металс. Оxфорд, УК & Амес, Иоwа: Блацкwелл Публисхинг. стр. 35—81. ИСБН 978-1-4051-1040-2. Приступљено 25. 6. 2012.
