Aluminijum hlorid
Appearance

| |
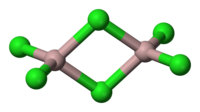
| |
| Nazivi | |
|---|---|
| IUPAC naziv
Aluminijum(III)-hlorid
| |
| Drugi nazivi
Aluminijum-trihlorid
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.028.371 |
| MeSH | Aluminium+chloride |
| UNII | |
| |
| |
| Svojstva | |
| AlCl3 | |
| Molarna masa | 133,34 g mol−1 (анхидрован) 241.432 g mol−1 (хексахидрат) |
| Agregatno stanje | bledožuta čvrsta supstanca, higroskopna supstanca. |
| Gustina | 2,48 g cm−3 |
| Tačka topljenja | 190°C 463 K) ispod 2.5 atm pritiska |
| Tačka ključanja | 178°C (451 K) (sublimira) |
| 43.9 g/100 ml (0°C) 44.9 g/100 ml (10°C) 45.8 g/100 ml (20°C) 46.6 g/100 ml (30°C) 47.3 g/100 ml (40°C) 48.1 g/100 ml (60°C) 48.6 g/100 ml (80°C) 49 g/100 ml (100°C) | |
| Struktura | |
| Kristalna rešetka/struktura | 6-koordinatna položena rešetka |
| Geometrija molekula | oktaedar (osnovno stanje) tetraedar (tečnost) |
| Oblik molekula (orbitale i hibridizacija) | trigonalna planarna (monomer u stanju pare) |
| Opasnosti | |
EU klasifikacija (DSD)
|
Korozivan (C) |
| R-oznake | R34 |
| S-oznake | (S1/2), S7/8, S28, S45 |
| Srodna jedinjenja | |
Drugi anjoni
|
Aluminijum-fluorid Aluminijum-bromid Aluminijum-jodid |
Drugi katjoni
|
Bor-trihlorid Galijum(III)-hlorid Indijum(III)-hlorid Talijum(III)-hlorid Magnezijum-hlorid |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |

Aluminijum hlorid AlCl3 je jedna od najvažnijih soli aluminijuma, koja nalazi primenu u organskim sintezama.[3][4] Aluminijum hlorid je veoma dobro rastvorljiv. Ovo jedinjenje pokazuje veoma jake kisele osobine. Relativna atomska masa ovog jedinjenja iznosi približno 133,34
Struktura
[uredi | uredi izvor]Aluminijum hlorid se sastoji od jednog atoma aluminijuma sa oksidacionim brojem +3 i od tri atoma hlora sa oksidacionim brojem -1.
Nalazi se u čvrstom agregatnom stanju
Izvori
[uredi | uredi izvor]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0911910131.
Literatura
[uredi | uredi izvor]- Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st izd.). San Diego: Academic Press. ISBN 0-12-352651-5.
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. izd.). Prentice Hall. ISBN 978-0-13-175553-6.
