Fluoroantimonska kiselina

| |
| Nazivi | |
|---|---|
| Preferisani IUPAC naziv
Fluoroantimonic acid | |
| Sistemski IUPAC naziv
Hydrogen hexafluoro-λ5-stibanuide | |
| Drugi nazivi
H(+) heksafluoro-λ5-stibanuid
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.037.279 |
| EC broj | 241-023-8 |
| |
| Svojstva | |
| HSbF6 | |
| Molarna masa | 236,808 g/mol |
| Agregatno stanje | bezbojni sirup |
| Gustina | g cm–3 |
| Tačka topljenja | °C na mmHg |
| Tačka ključanja | razlaže se |
| razlaže se | |
| Kiselost (pKa) | −25 |
| Opasnosti | |
| Opasnost u toku rada | korozivna |
| R-oznake | R26, R29, R35 |
| Tačka paljenja | nezapaljiva |
| Srodna jedinjenja | |
Drugi anjoni
|
HBF4 |
Drugi katjoni
|
NaPF6, NaSbF6 |
Srodne kiseline
|
HF SbF5 Magična kiselina |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Fluoroantimonska kiselina (HSbF6) predstavlja mešavinu fluorovodonika i antimon-pentafluorida u različitim odnosima. Kombinacija 1:1 formira najjaču poznatu superkiselinu, koja može da protonizuje i ugljovodonike pri čemu se dobiju karbokatjoni i H2.
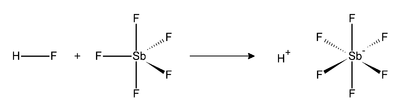
Reakcija između vodonikfluorida (HF) i SbF5 je egzotermna. HF oslobađa svoj proton (H+) i njegova konjugovana baza (F−) je uzeta od strane SbF5 pri čemu se dobije oktaedarni SbF6−. Ovaj anjon je klasifikovan kao nekoordinirajući, zato što je veoma slab nukleofil i veoma slaba baza. Proton efektivno postaje "go" što doprinosi velikoj kiselosti. Fluorantimonska kiselina je 2×1019 puta jača od 100% sumporne kiseline.
Struktura
[уреди | уреди извор]Iz mješavine HF-SbF5 su kristalizovana dva produkta, i oba su bila analizirana uz pomoć rendgenske analize kristala. Ove soli imaju formule [H2F+][Sb2F11−] i [H3F2+][Sb2F11−]. U obe soli postoji anjon Sb2F11−. Kao što je već rečeno SbF6− spada u slabe baze, a veći anjon Sb2F11− je još slabija baza.
Primjena
[уреди | уреди извор]Ova jaka kiselina protonizuje skoro sva organska jedinjenja. Pokazano je 1967. godine da će HF-SbF5 ukloniti H2 iz izobutana i metan iz neopentana:
- (CH3)3CH + H+ → (CH3)3C+ + H2
- (CH3)4C + H+ → (CH3)3C+ + CH4
Mjere opreza
[уреди | уреди извор]HF-SbF5 se razlaže sa vodom brzo i eksplozivno. Reaguje sa skoro svim rastvaračima. Rastvarač koji je kompatibilan sa HF-SbF5 je SO2ClF i tečni sumpor dioksid. Freoni su takođe koriste kao rastvarači. Posude za HF-SbF5 se prave od politetrafluoretilena.
Reference
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.