Хром-триоксид
Изглед
(преусмерено са Hrom trioksid)

| |
| |
| Називи | |
|---|---|
| IUPAC називs
Хром-триоксид
Хром(VI) оксид | |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.014.189 |
| MeSH | Chromium+trioxide |
| RTECS | GB6650000 |
| UNII | |
| UN број | 1463 |
| |
| |
| Својства | |
| CrO3 | |
| Моларна маса | 99,994 g/mol |
| Агрегатно стање | Тамноцрвена грануларна супстанца |
| Густина | 2,70 g/cm3 (20 °C), основно |
| Тачка топљења | 197 °C |
| Тачка кључања | 251 °C, распада се |
| 61.7 g/100 mL (0 °C) 63 g/100 mL (25 °C) 67 g/100 mL (100 °C) | |
| Растворљивост | раствара се у сумпорној и азотној киселини |
| Опасности | |
ЕУ класификација (DSD)
|
Оксидант (O) Carc. Cat. 1 Muta. Cat. 2 Repr. Cat. 3 Веома токсичан (T+) Опасан за животну средину (N) |
| R-ознаке | R45, R46, R9, R24/25, R26, R35, R42/43, R48/23, R62, R50/53 |
| S-ознаке | S53, S45, S60, S61 |
| NFPA 704 | |
| Смртоносна доза или концентрација (LD, LC): | |
LD50 (средња доза)
|
80 mg/kg |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
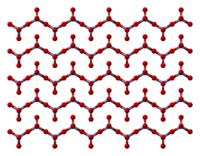
Хром-триоксид је оксид хрома хемијске формуле CrO3, где је оксидациони број хрома +3.
Добијање
[уреди | уреди извор]Може се добити реакцијом натријум-хромата[3] или калијум-дихромата и сумпорне киселине[4]:
Својства
[уреди | уреди извор]Ово је чврста супстанца затвореноцрвене боје, која постоји у облику призматичних игличастих кристала. На високој температури прво испарава, па се топи на 190 °C, при чему се већ делимично распада. При већој температури се распада на хроми-оксид и кисеоник[4]:
Слична реакција се врши и приликом редукције, јер је хром-триоксид веома јако оксидационо средство. Алкохол ће се у додиру са овим оксидом упалити, хартија угљенисати, а угаљ се оксидовати у угљен-диоксид. У вода|води се раствара лако, дајући највероватније полихромне киселине.[4]
| Особина | Вредност |
|---|---|
| Партициони коефицијент[5] (ALogP) | -0,1 |
| Растворљивост[6] (logS, log(mol/L)) | 0,3 |
| Поларна површина[7] (PSA, Å2) | 51,2 |
Референце
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ „Chromium Trioxide”. Chemicalland21.
- ^ а б в Паркес, Г. Д. & Фил, Д. 1973. Мелорова модерна неорганска хемија. Научна књига. Београд.
- ^ Ghose, A.K.; Viswanadhan V.N. & Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A. 102: 3762—3772. doi:10.1021/jp980230o.
- ^ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488—1493. PMID 11749573. doi:10.1021/ci000392t.
- ^ Ertl P.; Rohde B.; Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714—3717. PMID 11020286. doi:10.1021/jm000942e.
Литература
[уреди | уреди извор]- Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st изд.). San Diego: Academic Press. ISBN 0-12-352651-5.
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6.




