Тефлон
| |
| |
| Називи | |
|---|---|
| IUPAC назив
Поли(1,1,2,2-тетрафлуороетилен)[1]
| |
| Други називи
Флуон, поли(тетрафлуроетен), поли(дифлуорометилен), поли(тетрафлуороетилен), тефлон
| |
| Идентификација | |
| Абревијација | PTFE |
| ChEBI | |
| ChemSpider |
|
| ECHA InfoCard | 100.120.367 |
| KEGG[2] | |
| UNII | |
| Својства | |
| (C2F4)n | |
| Густина | 2200 kg/m³ |
| Тачка топљења | 327 °C |
| Топлотна проводљивост | 0,25 W/(m·K) |
| Опасности | |
| NFPA 704 | |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Политетрафлуороетилен (PTFE) је синтетички флуорополимер од тетрафлуороетилена који има бројне примене. Тефлон је заштићено име за материјале базиране на политетрафлуороетилену. Ово име је регистровало предузеће Хемоурс,[3] које се одвојило од Дупонта, где је овај материјал оригинално откривен 1938. године.[3] Тефлон је пронашао амерички хемичар Рој Џ. Планкет 1938. године.
Тефлон се добија слободнорадикалском полимеризацијом мешањем тетрафлуороетена са воденим раствором амонијум-персулфата. Може се добити суспензионом полимеризацијом или дисперзионом полимеризацијом (чиме се добија дисперзија полимера у води која се може концентровати и користити за премазе). Суспензионом полимеризацијом се добијају знатно веће честице, које се могу обликовати под притиском.
Употреба му се заснива на хемијској инертности, термалној стабилности и нелепљивости. Од посебног значаја за његову употребу је што се топи тек на 327 °C[4] па се може користити за кухињско посуђе. Тефлонизација материјала се изводи тако што се површина материјала механички учини неравном, а затим се шупљине под притиском испуњавају тефлоном.
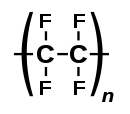
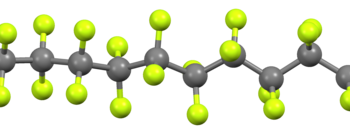
Хемијска структура
[уреди | уреди извор]
Предност тефлона у односу на остале материјале је што за њега ништа не пријања. Ова особина тефлона се објашњава великим бројем атома флуора који је најелектронегативнији елемент Периодног система. Електрони око флуора стварају штит око полимера и спречавају хемијска једињења да приђу полимеру. Поред тога, врло јака веза угљеник-флуор чини тефлон инертним те се користи у хемијској индустрији.
Примена
[уреди | уреди извор]
Међутим, његова нереактивност га чини проблематичним за примену јер је проблем нанети га на површину. Користи се за израду реактора или пресвлака у реакторима у којим се одигравају реакције са корозивним супстанцама, такође и као материјал за боце у којима се чувају суперкиселине. Од њега се израђују полупропустљиве мембране у хлор-алкалној индустрији, пермеабилне мембране (енгл. Gore-Tex) које пропуштају водену пару напоље, а не пропуштају воду у обућу, цеви за катетер, посуђе у домаћинству, а користи се и као чврсти лубрикант.
Извори
[уреди | уреди извор]- ^ „poly(tetrafluoroethylene) (CHEBI:53251)”. ebi.ac.uk. Приступљено 12. 7. 2012.
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ а б „The History of Teflon Fluoropolymers”. Teflon.com (на језику: енглески). Приступљено 2021-02-03.
- ^ „Teflon™ PTFE” (PDF).
Литература
[уреди | уреди извор]- Ellis, D.A.; Mabury, S.A.; Martin, J.W.; Muir, D.C.G.; Mabury, S.A.; Martin, J.W.; Muir, D.C.G. (2001). „Thermolysis of fluoropolymers as a potential source of halogenated organic acids in the environment”. Nature. 412 (6844): 321—324. Bibcode:2001Natur.412..321E. PMID 11460160. S2CID 4405763. doi:10.1038/35085548.
Спољашње везе
[уреди | уреди извор]- "EPA: Compound in Teflon may cause cancer", Tom Costello, NBC News, 29 June 2005. (Flash video required)
- "Teflon chemical cancer risks downplayed?", 30 June 2005
- Plasma Processes and Adhesive Bonding of Polytetrafluoroethylene
- PTFE (polytetrafluoroethylene) (Properties) | Fluorotherm.com
- PTFE at Holscot Fluoroplastics

