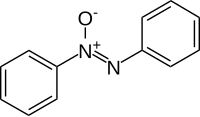
Азоксибензен
| |

| |
| Називи | |
|---|---|
| Преферисани ИУПАЦ назив
Дифенилдиазен оксид [1] | |
| Други називи | |
| Идентификација | |
| ECHA InfoCard | 100.007.094 |
| УНИИ | |
| Својства | |
| C12H10N2O | |
| Моларна маса | 198,23 г·мол−1 |
| Агрегатно стање | жута чврста супстанца |
| Густина | 1,318 g/cm3 |
| Тачка топљења | 35,5—36,5 °Ц (95,9—97,7 °Ф; 308,6—309,6 К) |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°Ц [77°Ф], 100 кПа). | |
| Референце инфокутије | |
Азоксибензен је органско једињење са формулом C6Х5Н(О)НЦ6Х5. То је жута чврста супстанца која има ниску тачку топљења. [4] Молекул има планарно језгро C2Н2О. Дужина НН и НО везе је скоро иста на 1,23 А. [5]
Припрема[уреди | уреди извор]
Може се припремити делимичним смањењем нитробензена. Ова реакција је предложена да се настави путем посредовања фенилхидроксиламина и нитрозобензена: [4]
- ПхНХОХ + ПхНО → ПхН(О)НПх + Х2О
Друга опција је оксидација анилина водоник-пероксидом у ацетонитрилу на 50 °Ц (122 °Ф; 323 К). У овој реакцији, пХ треба одржавати око 8, да би се активирао водоник-пероксид и истовремено избегло превише ослобађања кисеоника. Прво се оксидује ацетонитрил, формирајући имин хидропероксид. Затим, ова међуфаза оксидује анилин у азоксибензен. [4]
- ЦХ3ЦН + Х2О2 → [ЦХ3C(ООХ)=НХ]
- 2 ПхНХ2 + 3 [ЦХ3C(ООХ)=НХ] → ПхН(О)НПх + 3 ЦХ3C(О)НХ2 + 2 Х2О
- ПхНО2 + На3АсО3/НаОХ→ Пх−Н+О−=Н-Пх
Још једна од опција када се Азоксибензен добија редукцијом нитробензена са натријум арсенитом, који се, пак, добија растварањем арсеник(III) оксида у воденој бази. Након обраде, производ се издваја у облику жутих кристала. [6]
Својства[уреди | уреди извор]
Топлота разлагања одређена коришћењем ДСЦ је −258 кЈ мол−1 или −1303 кЈ кг−1. [7]
Хемијска својства[уреди | уреди извор]
Азоксибензен реагује са алуминијум хлоридом у ЦС2 или са ацетил хлоридом, дајући пара-хлоразобензен. Ако се иста реакција одвија у бензену, производи се само пара-фенилазобензен. [8]
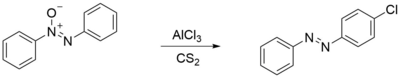
На сличан начин, азоксибензен реагује са алкил и арилсулфонил хлоридима, како би произвео заменске производе у пара положају са извесном додатком орто супституционог производа. Ако уместо сулфонил хлорида узмемо одговарајуће анхидриде, реакција доводи до стварања само парапроизвода. [8]

При реакцији са антимон(V) хлоридом долази до таложења комплекса чије топлотно распадање води до производа орто-хидроксилације. [8]

Референце[уреди | уреди извор]
- ^ а б в г Номенцлатуре оф Органиц Цхемистрy: ИУПАЦ Рецоммендатионс анд Преферред Намес 2013 (Блуе Боок). Цамбридге: Тхе Роyал Социетy оф Цхемистрy. 2014. стр. 1009. ИСБН 978-0-85404-182-4. дои:10.1039/9781849733069-00648.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б H. E. Bigelow; Albert Palmer (1931). „Azoxybenzene”. Organic Syntheses. 11: 16. doi:10.15227/orgsyn.011.0016.
- ^ S. P. G. Martínez; S. Bernès (2007). „trans-Diphenyldiazene Oxide”. Acta Crystallographica Section E. 63 (8): o3639. doi:10.1107/S1600536807035787.
- ^ Bigelow H. E., Palmer A. (1935). „Azoxybenzene”. Org. Syn (на језику: енглески). 11: 16. doi:10.15227/orgsyn.011.0016.
- ^ Grewer, T.; Klais, O.: Exotherme Zersetzung - Untersuchungen der charakteristischen Stoffeigenschaften, VDI-Verlag, Schriftenreihe "Humanisierung des Arbeitslebens", Band 84, Düsseldorf 1988, ISBN 3-18-400855-X, S. 9.
- ^ а б в EROS 2016.
Literatura[уреди | уреди извор]
- El-Awa A. (2016). „Azoxybenzene” (на језику: енглески) (Encyclopedia of Reagents for Organic Synthesis изд.). Wiley. doi:10.1002/047084289X.rn01782.

![{\displaystyle {\mathsf {PhNO_{2}{\xrightarrow[{NaOH,H_{2}O}]{As_{2}O_{3}}}PhN=N^{+}(O^{-})Ph}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/274dc1a1185c707bcb68d47e6855c0ce0f57382c)