Жива(I) јодид
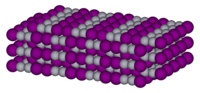
Изглед
| |
| Називи | |
|---|---|
| IUPAC назив
Жива(I) јодид
| |
| Други називи
Живин(I) јодид
| |
| Идентификација | |
3Д модел (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.035.811 |
| EC број | 239-409-6 |
| UN број | 1638 |
| |
| |
| Својства | |
| Hg 2I 2 | |
| Моларна маса | 654,99 g mol−1 |
| Агрегатно стање | тамножут |
| Мирис | безмирисан |
| Густина | 7,7 g Lm−1 |
| Опасности | |
| ГХС пиктограми |   
|
| ГХС сигналне речи | DANGER |
| H300, H310, H330, H373, H410 | |
| P260, P273, P280, P284, P301+310 | |
| Сродна једињења | |
Други анјони
|
Жива(I) флуорид Жива(I) бромид Жива(I) хлорид |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Жива(I) јодид је неоргански метални јодид који се забележава формулом Hg2I2. Добија се директним мешањем јода и живе. Лако се може распасти на живу и жива(II) јодид.
Синтеза
[уреди | уреди извор]Жива(I) јодид се може припремити путем директног комбиновања живе и јода:
- 2 Hg + I2 → Hg2I2
Структура
[уреди | уреди извор]Попут других Hg(I) једињења која садрже линеарне X-Hg-Hg-X јединице, Hg2I2 садржи IHg2I јединице са дужином Hg-Hg везе од 272 pm (Hg-Hg у металима је 300 pm) и дужином Hg-I везе од 268 pm.[3] Свеукупна координација сваког атома Hg је октаедрална, јер поред два најближа суседа, четири друга атома јода су на удаљености од 351 pm.[3] Ово једињење се често формулише као Hg22+ 2I−.[4]
Референце
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б Wells A.F. Structural Inorganic Chemistry 5th edition Oxford Science Publications. 1984. ISBN 978-0-19-855370-0.
- ^ Cotton F. Albert; Wilkinson Geoffrey; Murillo Carlos A; Bochmann, Manfred (1999). Advanced Inorganic Chemistry (6th изд.). New York: Wiley-Interscience. ISBN 0-471-19957-5.
