Згрушавање крви у крвном суду
| Згрушавање крви у крвном суду | |
|---|---|
 | |
| Класификација и спољашњи ресурси | |
| Специјалност | патологија васкуларна хирургија |
Згрушавање крви у шупљини крвног суда или тромбоза (од гр. речи θρόμβωσις thrómbōsis - згрушавање) заживотно је формирање угрушка крви (тромба) унутар крвних судова циркулационог систем, која за последицу има опструкцију (делимичну или потпуно зачепљење) и поремећај протока крви кроз нападнути крвни суд. Згрушавање крви у шупљини повређеног крвног суда треба разликовати о згрушавања крви које настаје изван кардиоваскуларног система када није пукнут крвни суд, или у кардиоваскуларном систему након смрти пацијента.
Када је крвни суд (вена или артерија) повређен, тело користи крвне плочице (тромбоците) и фибрин да формира угрушак крви како би спречио губитак крви. Међутим и када крвни суд није повређен, угрушци крви се могу формирати у телу због поремећаја метаболизма крви, нарушеног протока крви или оштећења ендотела крвног суда и изазвати зачепљење крвног суда.
Постоје два облика згрушавање крви у шупљини крвног суда: згрушавање крви у шупљини вена и згрушавање крви у шупљини артерија. Згрушавање крви у венама (понекад назвивано дубока венска тромбоза) доводи до формирања крвног угрушка и поремећаја венске дренађе у захваћеном делу тела, док згрушавање крви у артеријама утиче на снабдевање крвљу и доводи до оштећења ткива које се снабдевају из угрушком захваћене артерије (настаје исхемија и некроза). Део артеријског или венског тромба може да се одвоји као емболус, који затим путује кроз циркулацију и на месту на коме се задржи изазива емболију. Ова врста емболије је позната као тромбоемболија. Компликације могу настати када се венска тромбоемболија јави у плућима као плућна емболија,или ако се аертеријски емболус путујући низ захваћени крвни суд, заглави у неком виталном органу (среце, мозга, плућа).
Немачки лекар Рудолф Вирхов први је поставио постулат, да су потребна три предиспонирајући услова за формирање угрушка крви. Та три фактора су; оштећења зида крвног суда, нарушен проток крви и згрушавање крви. Знаци и симптоми овог синдрома зависе од врсте, величине и локације крвног угрушка, у ткивима и органима.[1]
Згрушавање крви (прелажење из чврстог у течно стање) једна је од физиолошких одлика организма, којом се он штити од патолошких процеса као што је то случај код крварења. Крв се нормално згрушава (коагулација) само изван крвних судова, када дође до повређивања његовог зида, јер организам на тај начин спречава губитак крви, заустављањем крварење. Цео процес почиње тако што, повреда зида крвног суда, активира бројне факторе (којих има 10) згрушавања крви у крвној плазми и ткивима. Под утицајем тих фактора ствара се ензим тромбопластин. Он активира протромбин, а потом тромбин који претвара течни фибриноген, из крвне плазме, у получврсте конце фибрина, који чине фину мрежицу (попут потке), око које се ствара угрушак крви, таложењем осталих елемената из крви (калцијума, крвних плочица, итд). Тако настаје чврста еластична маса коагулисане крви (коагулум) која санира оштећење на повређеном крвном суди и спречава даље крварење.
Епидемиологија
[уреди | уреди извор]- Морбидитет
На глобалном ниво, годишње се згрушавање крви у шупљини дубоких вена у Европи и САД јавља код око 50-160 људи на 100.000 становника, са смртношћу у око 0,06% популације.
У САД годишње се региструје око 275.000 нових случајева згрушавање крви у шупљини дубоких вена, са инциденцом првог јављања од 50,4 на 100.000 становника.
- Полне разлике
Венска обољења се чешће јављају код жена него мушкараца и тај однос се креће од 6:1 до 3:2. У Србији тај однос износи 5:2.
Згрушавање крви у шупљини дубоких вена у трудноћи је 6-10 пута чешћа код трудница у односу на остали део женске популације, а њена најтежа компликација - плућна емболија водећи је узрок смртности породиља. Згрушавање крви у шупљини дубоких вена код породиља се јавља код 0,1% до 0,7% свих трудница, и то не само у трећем триместру, него током целе трудноће.
Етиологија
[уреди | уреди извор]Хемостаза и њен значај
[уреди | уреди извор]
Хамостаза је нормалан физиолошки процес који спречава значајан губитак крви после васкуларне повреде. Процес хемостазе зависи од сложеног низа чинилаца, који укључују; тромбоците, друге ћелије крви и активирање одређених крвних протеина, познатих као фактори коагулације. Када дође до повреде крвних судова, физиолошка хемостаза се активира и процес коагулације јавља као физиолошки процес. Иако хаемостасис служи одржавању интегритета циркулаторног система; њен процес може постане неуравнотежен, што доводи до значајног морбидитета и морталитета изазваног тромбозом или тромбоемболијом.[2] Добро познавање процеса хемостазе је важно како би се разумели главни етиопатогенетски механизми болести повезаних са тромбозом, нпр венске тромбоемболије (ВТЕ), артериотромбоза (тромбоза изазвана руптуром атероматозног плака) и тромбоза срчаних крвних судова.
Процес коагулације који доводи до хемостазе обухвата сложен скуп реакција које укључују око 30 различитих протеина.[3] Ове реакције конвертује фибриноген у фибрин, који, заједно са тромбоцитима, формира стабилна тромб. За сада је предложено неколико модела каскадне коагулације, који укључујући спољашње и унутрашње процесе на ћелијском моделу. Ослањајући се на ове моде, у току истраживања разјашњена је улога и осталих чинилаца у процесу згрушавања, укључујући и микрочестице протеин П-селектина. Наследни или стечени поремећај у сложеном коагулационом систем доводи до повећаног ризика од тромбозе и тромбофилије. Отприлике један у три болесника са венском тромбозом (ВТЕ) има и наследну тромбофилију.[4]

Патолошка коагулација
[уреди | уреди извор]Патолошка коагулација или тромбоза, настаје у условима неравнотеже у система коагулације крви, и може потенцијално ометати проток крви, што доводи до више озбиљних здравствених поремећаја. Патолог Рудолф Вирхов први је описао најважније услове за настанка тромбозе и повезао их са неким од фактора ризика, јер тако створен тромб потенцијално може да омета проток крви, и довести до низа озбиљних здравствених проблема који укључују, срчаних напада и срчани и мождани удара код болесника са преткоморском или коморском фибрилацијом.[5][6][7]
| Промена особина крвног суда |
|
| Промена брзине циркулације крви |
|
| Промене у саставу крви |
|
Фактори ризика
[уреди | уреди извор]| Згрушавање крви у венама | Згрушавање крви у артеријама |
|---|---|
|
|
Врсте згрушавање крви у шупљини крвних судова
[уреди | уреди извор]Описано је неколико врста згрушавања крви у шупљини крвних судова које у зависности од њиховог настанка могу бити акутне или хроничне, од локализације угрушка крви у циркулацији артеријске или венске и системске.
Згрушавање крви у шупљини артерија
[уреди | уреди извор]
Као што јој сам назив каже изазвана је тромбом локализованим у артеријским крвним судовима. По начину настанка може бити акутна (нагла) и хронична (дуготрајна).
Покренути тромб (коагулум), настао у било ком делу циркулаторног система који се креће кроз крвни суд и бива заустављено обично на рачвама артерија, где доводи до стенозе или опструкције.
Најчешће, у око 85% случајева тромбоза је кардијалног порекла (кардиогени извор тромба) а у 10% екстракардијалног:
- Кардиогени извори крвног угрушка
- апсолутне или друге аритмије са стварањем коагулума у левој преткомори који пасивно прелазе у леву комору,
- постинфарктне анеуризме леве коморе,
- патолошке вегетације на валвулама (срчаним залисцима), миксоми,
- ендокардитис и паразитарна обољења.
- Екстракардијални извори крвног угрушка
- анеуризме аорте и других артерија где због турбулентног тока настају коагулуми који се покрећу пут дистално,
- улцерозни атеросклеротски плакови
- јатрогене емболије (откинути делови катетера, стентова или других материјала током дијагностичких и терапијских инвазивних поступака).
Згрушавање крви у шупљини артерија у највећем броју случајева изазива:
- Акутизација хроничног атеросклеротског процеса на ендотелу артерије — егзулцерација, интраплакална хеморагија, парцијално одлубљивање интиме, тромбоза анеуризме итд.
- Остали васкуларни процеси — артеритис, цистична медијална некроза, фибромускуларне дисплазија.
- Хематолошке болести — мијелопролиферативне болести, криоглобулинемије, тромбоцитопатије, коагулопатије.
- Посебна стања или болести — копалс, хиоповолемија, септикемија итд).
Код акутних тромбоза постоје опсежне патолошке промене ендотела што ова стања чини битно различитим од емболија где постоји мање или више очуван континуитет ендотела. Наиме, код тромбозе пре акутног процеса постојале су промене у зиду и колатерална мрежа.
Акутна згрушавање крви у шупљини артерије локално се компликује едемом зида крвног суда са миграцијом и нагомилавањем леукоцита што даље оштећује ендотел (унутрашњи зид крвног суда). Ове промене доводе до застоја крви, промене у коагулацији и формирање секундарног тромба. Тако створен секундарни тромб шири се у дисталном или проксималном правцу. На тај начин настају поремећаји у бочних гранама и колатералној циркулацији што може продубити степен исхемије и настанак анаеробног метаболизма (накупљање лактата и других анаеробних киселих метаболита) и последично доводи до поремећаја рада ћелијске мембране и оштећења натријумске и калијумске пумпе и интрацелуларне смрти.
Згрушавање крви у шупљини вена
[уреди | уреди извор]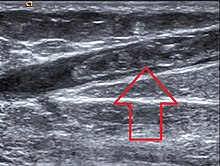
Згрушавање крви у шупљини вена изазвано је угрушком (тромбом) у површинским или дубоким венама. Венска обољења спадају у групу најмасовнијих обољења савременог човека. Јављају се у свим климатским условима, у свим расама и свим животним добима, а чешћа су код жена.
Могу имати:
- акутни (тромбоза дубоких вена - ТДВ, површински тромбофлебитис - СТФ, плућне емболије - ПТЕ)
- хронични ток - хронична венска инсуфицијенција - ХВИ (посттромботски синдром, дерматофлебосклероза, венски улкуси).
Згрушавање крви у шупљини крвног суда уопште, а посебно венско, је мултифакторијална болест у чијем настанку учествују најмање два фактора Вирховљеве тријаде. Њена етиопатогенеза базира на склоности згрушавању крви у шупљини вена и прогресивној дисфункцији венског система узрокованој валвуларном некомпетентношћу и/или венском опструкцијом, што доводи до ретроградног тока крви и венског рефлукса са прогресивним оштећењем микроциркулације.
Фактори ризика венских обољења су бројни и уклапају се у Вирхоов тријас:
- примарна обољења спољашњег зида и венских валвула (мезодермска астенија),
- застојна стања (статичко оптерећење)
- промене у саставу крви.[1]
Системско згрушавање крви
[уреди | уреди извор]- Хепарином изазвана тромбоцитопенија
Хепарином индукована тромбоцитопенија типа II (ХИТ II ) спада у групу леком индукованог поремећаја који се манифестују превасходно тромбозним манифестацијама, а чије препознавање и примена одговарајућих терапијских мера може имати кључну улогу у даљој прогнози болесника. Време изгубљено на чекање лабораторијске потврде ХИТ-а излже болесника ризику да се развију потенцијално опасне тромбозе, као и да се дијагноза ХИТ-а успоставља превасходно клинички.[1]
- Антифосфолипидни синдром
Овај синдрома је специфични аутоимунски поремећај који се клинички карактерише рекурентном (поваљајућом) тромбозом (венских и/или артеријских) крвних судова и/или рекурентним спонтаним побачајима, превременим порођајима и тромбоцитопенијом (смањеним бројем крвних плочица), са лабораторијски доказаним, перзистентно повишеним антифосфолипидним антителима.[а][8][9]
- Отекла плава нога
„Отекла плава нога” или „болни плави едем стање је слично отеклој белој нози, које настаје као последица нагло насталог акутног венског застоја проксималних дубоких вена (где нема услова за отварање колатерала).[10][11][12] То је посебна врста дубоке венске тромбозе у којој се удружено јављају проксимална венска тромбоза и знаци артеријске исхемије због бруталног и масовног едема и успоравања протока артеријске крви.[13]
Патофизиологија
[уреди | уреди извор]Угрушак крви настаје као резултат интравскуларне коагулације, која је повезана са тромбоцитима и коагулацијом плазме. Интраваскуларна, заживотна коагулација крви у принципу се одвија једнако као згрушавање крви ван организма.[14]
За разлику од физиолошке коагулације тромбоза очигледно представља згрушавање на погрешном месту, односно у непрекинутој крвној струју при оштећењу зида крвног суда, на коме се ствара тромбоцитни чеп, на који се надовезује коагулациони чеп[15].
Зато у тромбогенези разликујемо угрушак крви из тромбоцита и коагулациони угрушак крви.
За почетак формирања угрушак крви од пресудног је значаја непосредни контакт крвне плазме и тромбоцита са субендотелним колагеном. Ако на једном делу васкуларне мреже (артерије, вене, срце), увек због неког узрока, дође до оштећења ендотела ослобађа се ткивна тромбокиназа. Она у садејству са јонима калцијума доводи до стварања тромбина. Тромбин изазива вискозну метаморфозу тромбоцита, који се крећу у ивичној струји, при чему они аглутинирају и лепе се на месту оштећења ендотела. Тромбоцити покривају дефект за неколико секунди. У почетку тромбоцити се скупљају формирајући пруге, на чијим ивицама долази до новог таложења ових елемената и тиме раст почетних ламела у разгранате формације сличне коралима. На ово се таложе леукоцити и тако се проширује стварање тромба[16] [17]
Темпо изградње угрушак крви зависи од брзине струјања крви. Због тога се пораст угрушка у артеријама и у срцу спорије одвија него у венама, јер се делови тромбоцитних ламела откидају[18].
Распадањем тромбоцита опет се ослобађа тромбокиназа која поново која поново изазива стварање тромбина. Овај тромбин мења фибриноген плазме у фибрин, који сада гради густу влакнасту мрежу између ламела тромбоцитне коралене творевине и овај фибрин штрчи на ивицама ламела у виду чешља. Ова творевина одговара класичном белом тромбу, који је сув сивкасто-беличаст и на површини рапаво-пругастог изгледа. После формирања мрежног фибрина тромбоцити губе способност адхезије и нагомилавања. Због тога не долази до даљег повећања величине паријеталних тромба.
Ако се у насталу фибринску мрежу гомилају еритроцити, угрушак крви добија тракасти изглед, при чему су ламеле испупчене у виду чешља сиво беличасте боје, док поља између ламела имају црвенкасту боју услед присуства еритроцита. Тада говоримо о мешовитом тромбу.
Како на почетку интраваскуларног згрушавања крви услед оштећења ендотела долази до издвајања и нагомилавања тромбоцита, ово се означава као конглутинациони тромб. Он се чврсто држи за зид крвног суда попречно је избраздан, без сјаја, крт, показује сиво-беличасту или сивкасто-црвену боју.
Клиничка слика
[уреди | уреди извор]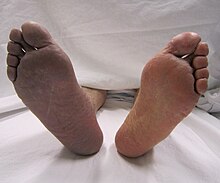
Клиничка слика згрушавања крви у крвном суду испољава се одређеним симптомима и знацима у зависно од врсте, величине и локализације процеса. Такође клиничка слика се разликује у зависности да ли се ради о артеријској или венској тромбози.
Згрушавање крви у артеријама
[уреди | уреди извор]Артеријске тромбозе узрокују смањен или потпуни престанак протока крви у ткиво или орган који та артерија васкуларизује.
- Згрушавање крви у коронарним артеријама испољава се симптомима и знацима пекторалне ангине или инфаркта миокарда.
- Згрушавање крви у централној артерије мрежњаче ока доводи до губитка вида.
- Згрушавање крви у бубрежним артерија испољава се болом у слабинском пределу, хематуријом, протеинуријом и хипертензијом.
- Згрушавање крви у мезентеријалним артеријама испољава се боловима у стомаку, муком, гађењем, повраћањем, проливом, губитком апетита и појавом крви у столици.
- Згрушавање крви у рачви аорте и артерија удова испољава се оклузивним појавама у виду наглог настанка јаког бола, Парестезија, анестезијом и парализом екстремитета. Кожа постаје хладна, бледа, местимично цијанотична са губиткомпулса. Ако се не спроведе одговарајуће лечење, настаје гангрена.
- Згрушавање крви у можданим артерија испољава се парезом или парализом, у зависноти од локализације тромба у централном нервном систему.
Згрушавање крви у венама
[уреди | уреди извор]Згрушавање крви у венама узрокују поремећај отицања крви из одређеног подручја.[19]
- Згрушавање крви у површним венама испољавају се болом, цијанозом и едемом захваћеног региона. Ако не наступи тромболиза, већ се тромб организује, настаје посттромбозни синдром који се најчешће јавља на доњим удовима. Испољава се трајним одржавањем отока и цијанозом. Застој отицања крви доводи до трофичних промена које се испољавају хиперпигментацијом, фиброзом и појавом гризлица на екстремитетима.
- Згрушавање крви у хепатичним венама испољава се болом у десном хипохондријум, увећањем јетре и појавом асцитеса. Жутица и спленомегалија настају код трећине пацијената. Згрушавање крви у портној вени праћена је појавом асцитеса, хематемезом и меленом, због крварења из проширених вена једњака или желуца и увећањем слезине.
- Згрушавање крви у плућним венама често угрожава живот пацијената.
Дијагноза
[уреди | уреди извор]
Дијагноза згрушавања крви у артеријским и венским крвним судовима поставља се на основу симптома и знакова зависно од врсте згрушавања и њене локализације. Поред клиничких знакова, згрушавање крви у крвним суду може се дијагностиковати ултразвучним,[20] сцинтиграфским, ангиографским и лабораторијским методама.
- Лабораторијски тестови крви
Лабораторијска дијагностика заснива се на специфичним имунским и функционалним тестовима којима се одређују најчешћи чиниоци тромбофилије и бројни молекулски обележивачи. Они представљају делове молекула или комплексе молекула, који настају као производ активирања тромбоцита, коагулације и фибринолизе.
- Сликовне методе
- Ултразвучна дијагностика која користи звучне таласе да провери проток крви у артеријама и венама.
- Венографија, која користи рендгенске зрака и контрестно средство убруизгано у вену за приказивање проток крви и тражење угрушака.
- Магнетна резонантна томографија и компјутеризована томографија, користе се у зависности од врсте угрушка крви и његове локализације.
Терапија
[уреди | уреди извор]Терапија је усмерен у више праваца; реканализација крвног суда, лечење компликација, спречавање поновног јављања тромба. Међутим без обзира на врсту и тежину компликација, камен темељац у лечењу тромбозе је тромболиза или уклањање крвног угрушка и спречавање његовог поновног јављања.
Реканализација крвног суда
[уреди | уреди извор]Растварање тромба
[уреди | уреди извор]
За реканализацију крвног суда растварањем тромба користе се антикоагуланти и тромболитички лекови који имају за циљ да у што краћем времену растворе угрушак (тромб), успоставе стабилан проток крви у зачепљеном крвном суду и спрече његово поновно јављање. Међутим, резултати лечења тромболитичком терапијом, у поређењу са хепарин антикоагулантном терапијом зависи од врсте „нападнутог” органа, и протеклог времена од појаве тромбозе до њихове примене.
Примена тромболитичке терапије најбоље резултате даје у следеће четири основне категорије тромбозе; дубока венска тромбоза, плућна емболија, акутне оклузије периферних артерија, акутни инфаркт миокарда. Одлуку за примену ове терапије треба донети тек након појединачне процене болесника, јер постоји стална опасност од крварења (посебно опасних код интракранијалних крварења).
Међутим примена антикоагулантне терапије као и тромболитичке захтева рутинско праћења интернационалног нормализованог однос (енгл. international normalized ratio) као мерила спољашњег пута коагулације (ИНР).[б][21]
| Тромболитичка терапија |
|
| Антикоагулантна терапија хепарином |
|
Хируршко уклањање тромба (тромбектомија)
[уреди | уреди извор]
Хируршка тромбектомија постиже се посебном техником примене Фогартијев балон катетера, којим се тромб комплетно уклања из авалвуларног, углавном фемороилијакалног сегмента уз накнадну примену антикоагулантне терапије. Интервенција се изводи у општој ендотрахеалној, спиналној, епидуралној или локалној анестезији, у условима опште хепаринизације и антибиотске профилаксе.[22]
По завршеној тромбектомији препоручује се формирање привремене (4 до 6 недеља) артериовенске фистуле која повећава проток кроз тромбектомисани сегмент и на тај начин спречава непосредну ретромбозу, доводи до бржег опоравка и јачања ендотела.
Примена хируршке тромбектомије код правилно изабраних болесника (нпр илијакофеморална тромбоза стара 24 до 48 сати) доводи до квалитетније тромболизе и реканализације крвног суда, и ти резултати су знатно бољи у односу на друге методе лечења.[23]
Лечење компликација
[уреди | уреди извор]- Лечење компликација код венске тромбиозе удова, као што су оток и бол у нози, спроводи се ношењем еластичних чарапа за вене и нестероидним антиинфламаторним лековима (НСАИЛ).
- Инфаркт миокарда лечи се применом централних аналгетика, нитроглицерина и мерама реанимације у критичним стањима.
- Плућне тромбоемболије лечи се применом кисеоника преко маске и другим мерама реанимације, антибиотицима и другом симптоматском терапијом.
Превенција
[уреди | уреди извор]За спречавање стварања угрушка крви користе се антикоагуланси (хепарин и антагонисти витамини К), инхибитори агрегације тромбоцита и фибринолитици (урокиназа, стрептокиназа и алтеплаза).[24]
Како антицоагуланти немају утицати на већ формиране угрушка крви, уклањање угрушка крви из крвног суда може се постићи једино фибринолизом (у којој се хидролизује фибрин), по својим механизмима дејства, процесом супротним од коагулације.[25] Зато је процес фибринолизе једнако важан за организам као и процес коагулације. Фибринолизу и тромболизу покрећу плазминогени активатори ( ендогена тромболитичка средства) као што урокиназа и ткивни плазминогени активатор. Они конвертују плазминоген у плазмин, ендопептидазу која раствара фибрин. Код ове терапије могуће су компликације у виду крварење у другим органима (нпр цереброваскуларна и гастроинтестинална).[26]
Ниже дозе антикоагуланса хепарина користе се у:[24]
- превенцији венске тромбоемболије,
- код болесника са високим ризиком од тромбозе,
- код болесника са конгестивном инсуфицијенцијом срца,
- код болесника након срчаног удара и код кардиомиопатије.
Напомене
[уреди | уреди извор]Извори
[уреди | уреди извор]- ^ а б в Максимовић Ж. и сар, Акутна и хронична обољења вена Водич за дијагностиковање и лечење акутних и хроничних обољења вена. Београд, Ниш, Нови Сад, Крагујевац Грешка код цитирања: Неисправна ознака
<ref>; назив „:0” је дефинисано више пута с различитим садржајем - ^ Heit, J. A. (2005). „Venous thromboembolism: Disease burden, outcomes and risk factors”. J Thromb Haemost. 3 (8): 1611—1617. PMID 16102026. S2CID 22341180. doi:10.1111/j.1538-7836.2005.01415.x..
- ^ Colman RW, Clowes AW, George JN et al. Overview of coagulation, fibrinolysis and their regulation. In Hemostasis and Thrombosis: Basic Principles and Clinical Practice. 5th edn. Colman RW, Clowes AW, George JN et al. (editors). Philadelphia: Lippincott, Williams & Wilkins; 2006. pp. 17–20.
- ^ Colman RW, Clowes AW, George JN et al. Overview of hemostasis. In Hemostasis and Thrombosis: Basic Principles and Clinical Practice. 5th edn. Colman RW, Clowes AW, George JN et al. (editors). Philadelphia: Lippincott, Williams & Wilkins; 2006. pp. 1–16.
- ^ Tapson, V. F. (2008). „Acute pulmonary embolism”. New England Journal of Medicine. 358 (10): 1037—1052. PMID 18322285. S2CID 40243031. doi:10.1056/NEJMra072753..
- ^ Lyaker, M. R.; Tulman, D. B.; Dimitrova, G. T.; Pin, R. H.; Papadimos, T. J. (2013). „Arterial embolism”. Int J Crit Illn Inj Sci. 3 (1): 77—87. PMC 3665125
 . PMID 23724391. doi:10.4103/2229-5151.109429
. PMID 23724391. doi:10.4103/2229-5151.109429  ..
..
- ^ Fuster, V.; Moreno, P. R.; Fayad, Z. A.; Corti, R.; Badimon, J. J. (2005). „Atherothrombosis and high-risk plaque: Part I: Evolving concepts”. J Am Coll Cardiol. 46 (6): 937—954. PMID 16168274. doi:10.1016/j.jacc.2005.03.074..
- ^ Giannakopoulos, B.; Passam, F.; Rahgozar, S.; Krilis, S. A. (2007-01-15). „Current concepts on the pathogenesis of the antiphospholipid syndrome”. Blood. 109 (2): 422—30. PMID 16985176. S2CID 21287913. doi:10.1182/blood-2006-04-001206.
- ^ Triona Holden (2003). Positive Options for Antiphospholipid Antibody Syndrome. Hunter House. ISBN 978-0-89793-409-1.
- ^ Perkins JM, Magee TR, Galland RB. Perkins, J. M.; Magee, T. R.; Galland, R. B. (1996). „Phlegmasia caerulea dolens and venous gangrene”. Br J Surg. 83 (1): 19—23. PMID 8653352. S2CID 35970985. doi:10.1002/bjs.1800830106..
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомBrowse. - ^ Ginsberg JS. Peripheral venous disease. In: Goldman L, Schafer AI, eds. Goldman's Cecil Medicine. 25th ed. Philadelphia, PA: Elsevier Saunders; 2016:chap 81.
- ^ Lim W. Venous thromboembolism. In: Hoffman R, Benz EJ, Silberstein LE, Heslop HE, Weitz JI, Anastasi J, eds. Hematology: Basic Principles and Practice. 6th ed. Philadelphia, PA: Elsevier; 2013:chap 144.
- ^ Furie, Bruce; Furie, Barbara (2008). „Mechanisms of Thrombus Formation”. The New England Journal of Medicine. 359 (9): 938—949. PMID 18753650. doi:10.1056/NEJMra0801082.
- ^ Furie, Bruce; Furie, Barbara (2008). „Mechanisms of Thrombus Formation”. The New England Journal of Medicine. 359 (9): 938—949. PMID 18753650. doi:10.1056/NEJMra0801082.
- ^ Dubois C, Panicot-Dubois L, Merrill-Skoloff G, Furie B, Furie BC. Glycoprotein VI-dependent and -independent pathways of thrombus formation in vivo.. Dubois, C.; Panicot-Dubois, L.; Merrill-Skoloff, G.; Furie, B.; Furie, B. C. (2006). „Glycoprotein VI-dependent and -independent pathways of thrombus formation in vivo”. Blood. 107 (10): 3902—3906. PMC 1895285
 . PMID 16455953. doi:10.1182/blood-2005-09-3687.
. PMID 16455953. doi:10.1182/blood-2005-09-3687.
- ^ (језик: енглески) Mangin P, Yap CL, Nonne C, et al. Thrombin overcomes the thrombosis defect associated with platelet GPVI/FcRgamma deficiency.. Mangin, P.; Yap, C. L.; Nonne, C.; Sturgeon, S. A.; Goncalves, I.; Yuan, Y.; Schoenwaelder, S. M.; Wright, C. E.; Lanza, F.; Jackson, S. P. (2006). „Thrombin overcomes the thrombosis defect associated with platelet GPVI/FcRgamma deficiency”. Blood. 107 (11): 4346—4353. PMID 16391010. doi:10.1182/blood-2005-10-4244.
- ^ Dubois, C.; Panicot-Dubois, L.; Gainor, J. F.; Furie, B. C.; Furie, B. (2007). „Thrombin-initiated platelet activation in vivo is VWF independent during thrombus formation in a laser injury model”. The Journal of Clinical Investigation. 117 (4): 953—960. PMC 1821068
 . PMID 17380206. doi:10.1172/JCI30537.
. PMID 17380206. doi:10.1172/JCI30537.
- ^ Maksimović Ž: Bolesti vena. Medicinski fakultet, CIBID, Beograd, 1998.
- ^ Wulff, C.; Lorentzen, T.; Christensen, E.; Pedersen, E. B. (1996-11-11). „Phlegmasia alba dolens diagnosed with Doppler ultrasonography”. Ugeskr Laeger. 158 (46): 6623—4. PMID 8966831..
- ^ Prandoni P, Bernardi E. Upper extremity deep vein thrombosis. Curr Opin Pulm Med 1999; 5:222.
- ^ Yang, F.; Huang, P. C.; Yan, L. L.; Zhang, Z. D.; Fu, Y. F.; Xia, F. F. (август 2019). „Catheter Aspiration With Recanalization for Budd-Chiari Syndrome With Inferior Vena Cava Thrombosis”. Surg Laparosc Endosc Percutan Tech. 29 (4): 304—307. PMID 30629033. S2CID 58643989. doi:10.1097/SLE.0000000000000624..
- ^ Maksimović Ž: Tromboza dubokih vena – profilaksa i lečenje. Zavod za udžbenike i nastavna sredstva, Beograd, 1996.
- ^ а б Romantsik, Olga; Bruschettini, Matteo; Zappettini, Simona; Ramenghi, Luca Antonio; Calevo, Maria Grazia (2016-11-07). „Heparin for the treatment of thrombosis in neonates”. Cochrane Database of Systematic Reviews. 2016 (11): CD012185. ISSN 1465-1858. PMC 6464761
 . PMID 27820879. S2CID 42639740. doi:10.1002/14651858.cd012185.pub2.
. PMID 27820879. S2CID 42639740. doi:10.1002/14651858.cd012185.pub2.
- ^ Bi Y, Chen H, Zhang W, Ren J, Han X. Treatment of aortic thrombosis with retrievable stent filter and thrombolysis: a case report. BMC Cardiovasc Disord. 2019 Mar 05;19(1):54.
- ^ Ellen C Keeley, Judith A Boura, Cindy L Grines (4. 1. 2003). Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. The Lancet 361: 13–20.
Спољашње везе
[уреди | уреди извор]| Класификација |
|---|
- Msd-priručnici, Duboka venska tromboza
- A Venous & Arterial Thrombosis Resource For Physicians
- Antifosfolipidni sindrom (APS) Архивирано на сајту Wayback Machine (26. март 2021)
 | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |
