Жива(I) нитрат
Изглед
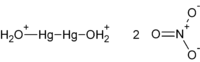
| |
| Називи | |
|---|---|
| IUPAC назив
Živa(I) nitrat
| |
| Други називи
Живин нитрат
| |
| Идентификација | |
| ECHA InfoCard | 100.202.814 |
| Својства | |
| Hg2(NO3)2 (anhydrous) Hg2(NO3)2·2H2O (dihydrate) | |
| Моларна маса | 525,19 g/mol (anhidrat) 561,22 g/mol (dihidrat) |
| Агрегатно стање | Бели кристали (анхидрат) безвојни кристали (дихидрат) |
| Густина | ? g/cm3 (anhidrat) 4,8 g/cm3 (dihidrat) |
| Тачка топљења | ? (anhidrat) razlaže se na 70°C (dihidrat) |
| незнатно растворан, реактиван | |
| Опасности | |
| НФПА 704 | |
| Сродна једињења | |
Други ањони
|
Жива(I) флуорид Жива(I) хлорид Жива(I) бромид Жива(I) јодид |
Други катјони
|
Жива(II) нитрат |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
Жива(I) нитрат је хемијско једињење са формулом Hg2(NO3)2. Оно се користи у припреми других жива(I) једињења, и попут других живиних једињење је токсично.
Реакције
[уреди | уреди извор]Жива(I) нитрат се формира комбиновањем живе са разблаженом азотном киселином (концентрована азотна киселина би произвела жива(II) нитрат). Жива(I) нитрат је редукујући агенс који се оксидује у контакту са ваздухом.
Раствори жива(I) нитрата су кисели услед споре реакције са водом:
- Hg2(NO3)2 + H2O → Hg2(NO3)(OH) + HNO3
Hg2(NO3)(OH) формира жути талог.
Ако се раствор загреје до кључања или изложи светлости, жива(I) нитрат подлеже реакцији диспропорционације производећи елементарну живу и жива(II) нитрат[2]:
- 2Hg2(NO3)2 → Hg + Hg(NO3)2
Референце
[уреди | уреди извор]- ^ Лиде, Давид Р. (1998), Хандбоок оф Цхемистрy анд Пхyсицс (87 изд.), Боца Ратон, ФЛ: ЦРЦ Пресс, стр. 4—45, ИСБН 978-0-8493-0594-8
- ^ а б Патнаик, Прадyот (2003), Хандбоок оф Инорганиц Цхемицал Цомпоундс, МцГраw-Хилл Профессионал, стр. 573, ИСБН 978-0-07-049439-8, Приступљено 20. 7. 2009

