Infektivni endokarditis
| Infektivni endokarditis | |
|---|---|
| Sinonimi | Bakterijski endokarditis |
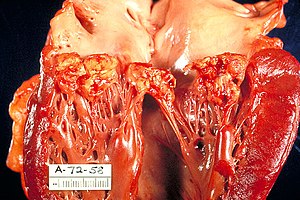 | |
| Vegetacije na mitralnim valvulama kod bakterijskog endokarditisa | |
| Specijalnosti | kardiologija, infektologija |
| Simptomi | temperatura, petehijalna krvarenja, šum na srcu, malaksalost, anemija[1] |
| Komplikacije | insufivcijencija valvula, srčani zhastoj, srčani udar, insuficijencija bubrega[1][2] |
| Uzroci | bakterijska infekcija, gljivična infekcija[1] |
| Dijagnostički metod | klinička slika, kultura krvi, ehokardiografija[1] |
| Lečenje | antibiotici, hirurško lečenje[1] |
| Prognoza | 25% smrtni ishod[3] |
| Frekvencija | 5 na 100.000 godišnje[3] |
Infektivni endokarditis je zapaljenje unutrašnji sloja srčanog zida, najčešće izazvano bakterijama (streptokoke i stafilokoke) ili gljivicama. Može se javiti u bilo kojom periodu života, dva puta češće kod muškarca nego kod žene. Najvećem riziku izloženi su intravenski narkomani i imunokompromitovani bolesnici.[4][5][6][7]
Kliniču sliku karakteriše, visoka temperatura, šumovi na srcu, petehijalno krvarenja po koži, anemija, embolija i endokardne vegetacije (koje mogu dovesti do nekompentencije ili opstrukcije srčanih zalistaka, apscesa miokarda ili mikotične aneurizme.[8][9]
Dijagnoza se postavlja izolacijom uzročnog mikroorganizma iz krvi,[10] i ehokardiografijom. Leči se dugotrajnijom primenom antibiotika, a ponekad i hirurškim zahvatom,[11][12] ili nakon stomatoloških zahvata.[13]
Epidemiologija
[уреди | уреди извор]Nekad su od infektivnog endokarditis obolevali mladi pacijenti, sa jasno definisanom slikom bolesti srčanih valvula, uglavnom uzrokovanom reumatičnom bolešću. Danas, od infektivnog miokarditis obolev populacije odmakle životne dobi, i to najčešće posle neke (invazivne) medicinske dijagnostičko-interventne ili jatrogene procedure, kod bolesnika koji, prethodno, nisu imali oboljenje srčanih zalistaka ili imaju već implantiranu veštačku valvulu. Jedan od vodećih uzroka, danas, je i sve veća zloupotreba intravenski ubrizganih lekova, kao učestalost interventnih medicinskih procedura i intravenske terapije.[14]
U Sjedinjenim Američkim Državama najčešći uzrok nastanka infektivnog endokarditisa izazvanog bakterijama iz grupe Staphylococcus aureus su hemodijaliza, šećerna bolest intravaskularni implantati (kateteri, stentovi...),[15] a u drugim razvijenim zemljama zloupotreba intravenskog unošenja lekova.[16]
Na globalnom nivou incidenca infektivnog endokarditisa, varira od zemlje do zemlje, i kreće se u rasponu od 3-10 na 100.000 osoba godišnje, sa niskom učestalošću bolesti u mlađoj populaciji, i značajnim porastom incidence u popolaciji odmakle životne dobi (70-80 godina), koja je i do 145 na 100.000 osoba godišnje.[17] Povećana učestalost zaraznog endokarditisa kod osoba starijih od 65 godina, je verovatno uzrokovana većim brojem faktora rizika za infektivni endokarditis.[18][19]
Godišnja incidencija infektivnog endokarditisa je veća kod muškaraca nego kod žena, sa muško:ženskim odnosom 2:1.
Iako istorija bolesti zalistaka ima značajnu povezanost sa infektivnim endokarditisom, 50% svih slučajeva razvija se kod pacijenata koji nemaju poznatu valvularnu bolest.[20][21]
Etiopatogeneza
[уреди | уреди извор]Endokarditis je uzrokovan bakterijama u krvotoku koje se umnožavaju i šire preko unutrašnje obloge srca (endokarda). Endokardijum se upali, što dovodi do oštećenja srčanih zalistaka.Vaše srce je obično dobro zaštićeno od infekcije tako da bakterije mogu bezopasno proći. Ako su srčani zalisci oštećeni ili su ugrađeni veštački zalistci, bakterijama je lakše da se ukorene i zaobiđu normalan imuni odgovor na infekciju.[22][23]
Na mestu infekcije mogu se razviti male nakupine bakterija. Postoji rizik da ove grudvice deluju na sličan način kao krvni ugrušci, oni putujući dalje od srca blokiraju dotok krvi u organe. Ovo može izazvati otkaz organa ili izazvati moždani udar.[24]

Endotel srčanih zalistaka u zdravom organizmu je otporan na kolonizaciju i infekciju bakterijama koje su prisutne u cirkulaciji.[25] Međutim, u uslovima mehaničkog oštećenje endotela dolazi do ekspozicije subendotelnih slojeva, i matriks proteina, aktivaciji tkivnog faktora i trombocita, agregacije trombocita i formiranja fibrina.[26] Ovaj, inače normalan proces zarastanja, kod nebakterijskih trombotičnih endokarditisa kao i drugih oštećenja endokarda kateterima, elektrodama (pejsmejkera, kardioverter defibrilatora), reumatodinim i drugim degenerativnim promena, laminarni tok krvi čine turbulentnim. Turbulentni tok krvi potom stimuliše agregaciju trombocita i agregaciju bakterija prisutnih u cirkulaciji.[27]
Infalamatorna aktivacija endotela aktivira integrine tipa β1 koji se vezuje cirkulišući fibronektin za endotel. Streptokokus aureus i drugi izazivači infektivnog endokarditisa nose fibronektin vezujuće proteine kojima se spajaju za mesto lezije. Istovremeno, aktivira se i sistemski inflamatorni odgovor.[28]
Podela
[уреди | уреди извор]Infektivni endokarditis prema mestu infekcije i prema prisustvu intrakardijalnog ugrađenog materijala
[уреди | уреди извор]1. IE nativnih valvula levog srca,
2. IE veštačkih valvula levog srca,
- 2.1. Rani < 1 godine
- 2.2. Kasni > 1 g odine
3. IE desnog srca
4. IE izazvan implantacijom arata (pejsmejkera, kardioverter defibrilatora).[29]
Infektivni endokarditis prema mikrobiološkim nalazima
[уреди | уреди извор]1. Infektivni endokarditis sa pozitivnom hemokulturom različitih izazivača: streptococci i enterococci (gotovo uvek osetljivi na penicilin); staphylococci (uobičajeno je nfektivni endokarditi nativne valvule uzrokovana S aureus-om).[30][31][32]
2. Infektivni endokarditis sa negativnom hemokulturom zbog prethodne antibiotske terapije;
4. Infektivni endokarditis često udružen sa negativnim hemokulturama, najčešće streptococci, fastidious G-I haemophilus grupe.
5. Infektivni endokarditis sa stalno negativnim hemokulturama: Coxiella burnetii, Bartonella, Chlamydia.[33][29]
IE po obliku nastanka
[уреди | уреди извор]1. IE izazvan medicinskim tretmanom
- 1.1. Nozokomijalni - Nastanak IE u pacijenata hospitalizovanih > 48 h pre nastanka simptoma/kl slike
- 1.2. Nenozokomijalne - Znaci i simptomi IE kod pacijenta < 48 h posle prijema posle medicinske intervencije
- 1.2.1. Posle kućne nege, iv terapije, hemodijalize ili iv hemoterapije < 30 dana pre početka znakova IE;
- 1.2.2. Hospitalizacija na urgentna odeljenja < 90 d. Pre prvih simptoma IE ili
- 1.2.3. Smeštaj u domovima za negu
2. Vanbolnički IE - Znaci i/ili simptomi IE kod < 48 h posle prijema kod pacijenat koji nisu bili izloženi medicinskoj intervenciji.[34]
3. IE kod zloupotrebe iv lekova IE kod aktivnih korisnika IV lekova bez alternativnog izvora infekcije.[35]
Aktivni IE
[уреди | уреди извор]1. Sa perzistentnom temperaturom i pozitivnom hemokulturom
2. Sa aktivnom inflamatornom morfologijom utvrđenom tokom operacije
3. Sa antibiotskom terapijom u toku
4. Sa histopatološki potvrđene aktivnosti
Rekurentni
[уреди | уреди извор]1. Relaps - Ponovljene epizode IE istim uzročnikom < 6 meseci posle inicijalne epizode
2. Reinfekcija - Ponovljene epizode IE istim uzročnikom > 6 meseci posle inicijalne epizode
Klinička slika
[уреди | уреди извор]Simptomi endokarditisa mogu se razviti brzo tokom nekoliko dana (akutni endokarditis), ili polako tokom nekoliko nedelja ili možda meseci (subakutni endokarditis). Subakutni endokarditis je češći kod ljudi sa urođenim srčanim oboljenjima.[36]
- Akutni oblik (ABE)
Akutni oblik počinje naglo, kao sepsa, sa visokom temperaturom, groznicom, kod osoba koje su prethodno bile relativno zdrave. Ubrzo se javljaju komplikacije kao što su embolije, razvoj srčane insuficijenije, multiple petehije (crvene tačkice) po koži. A kod infektivnog endokarditis desnog srca – zapaljenja i apscesi pluća.[37]
- Subakutni oblik (SBE)
Subakutni oblik počinje simptomima opšte infekcije, kod osoba koje su već srčani bolesnici. Kliničkom slikom dominiraju temperatura, zamor, anoreksija, slabost, gubitak u težini, pospanost, stanje slično gripu, glavobolja, bol u zglobovima, grozničavo stanje, otežano disanje, bol u grudima, lupanje srca, bol u trbuhu, u predelu bubrega, krv u mokraći.
Drugi oblik započinjanja subakutnog infektivnog miokarditisa karakteriše sa razvojem komplikacija kao što su embolije moždanih arterija sa hemiplegijom (oduzetost polovine tela), infarktom bubrega ili slezine, bleda boja kože i vidljivih sluzokoža ili boja bele kafe, sa promenama na koži u vidu petehija.[38]
- Endokarditis veštačkih zalistaka (PVE)
Ovaj oblik enfokardita razvija se u 2–3% bolesnika u prvoj godini nakon zamene valvule i u 0,5% slučajeva godišnje nakon toga. Nešto je češći nakon zamene aortne nego mitralne valvule, a podjednako se javlja kako kod mehaničke tako i kod biološke valvule.[39]
Rane infekcije se javljaju ubrzo nakon hirurške ugradnje zalistaka (< 2 meseca) najčešće su posledica kontaminacije tkom operacije bakterijama rezistentnim na antibiotike (npr S. epidermidis, difteroidi, koliformni bacili, Candida spp., Aspergillus spp.).
Kasne infekcije nastaju kasnije, i uglavnom su posledica kontaminacije manje virulentnim mikroorganizmima za vreme operacije, ili prolazne asimptomatske bakterijemije, Najčešće su izazvane streptokokima; S. epidermidisom, difteroidima i anaerobnim gram–negativnim bacilima, Haemophilus spp., Actinobacillus acctinomycetemcomitans i Cardiobacterium hominis.
Dijagnoza
[уреди | уреди извор]Dijagnoza infektivnog endokarditisa je realativno laka kod bolesnika sa klasičnom kliničkom slikom: bakteriemija ili fungiemija, sa oboljenjem valvula, perifernim embolijama i imunološkim vaskularnim promenama.[40] Međutim, koda akutnog toka infektivnog endokarditisa periferni znaci su retki ili izostaju, dok kod narkomana i osoba koje zloupotrebljavaju intravenski put, infektivni endokarditis je posledica infekcije bakterijom Stafilokokus aureus sa kliničkom slikom oboljenja valvula desnog srca.[4][41][42]
Dijagnoza infektivnog endokarditisa se postavlja na osnovu;[43][44]
- Kulture krvi i drugih laboratorijskih testova
- Ehokardiografiji i ponekad i drugim modalitetima snimanja
- Kliničkih kriterijuma
Kultura krvi
[уреди | уреди извор]Osim pozitivnih krvnih kultura, nema posebnih laboratorijskih nalaza. Utvrđene infekcije često uzrokuju normocitno-normohromnu anemiju, povišen broj belih krvnih zrnaca, povećanu brzinu sedimentacije eritrocita, povećani nivo imunoglobulina i prisustvo cirkulirajućih imunih kompleksa i reumatoidnog faktora, ali ovi nalazi nisu od dijagnostičke pomoći.
Analiza urina često pokazuje mikroskopsku hematuriju, a povremeno i odljeve crvenih krvnih zrnaca, piuriju ili bakteriuriju.
Ehokardiografija
[уреди | уреди извор]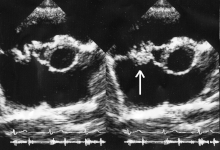
Transtorakalna,[45] i transoezofagealna,[46] ehokardiografija (TTE / TEE) su sada sve prisutnije i značajne dijagnostičke metode u dijagnozi, terapiji i praćenju IE.[47] Ehokardiografija se mora izvesti što pre čim se posumnja na IE.[48]
Korisnost oba načinadijagnostike je umanjena kada se primenjuje neselektivno, a odgovarajuća primena u kontekstu jednostavnih kliničkih kriterijuma poboljšava dijagnostiku.[49] Izuzetak je pacijent sa bakterijemijom izazvanom S. aureus u kojoj je opravdana rutinska ehokardiografija, jer je učestalost IE u ovom okruženju i virulencija ovog mikroorganizma velika kao i njegovi razarajući efekti nakon što se intrakardijalna infekcija uspostavljen.[50][51]
Tri najvažnija ehokardiografska nalaza, koji su glavni kriterijumi u dijagnozi IE su:[52]
- vegetacije (vidi sliku),
- apsces,
- dehiscencija valvula.
Klinički kriterijumi
[уреди | уреди извор]
Budući da su simptomi i znakovi nespecifični, uvelike se razlikuju i mogu se podmuklo razviti, dijagnoza zahtijeva visok indeks sumnje. Na endokarditis treba sumnjati kod pacijenata s vrućicom i bez očiglednog izvora infekcije, posebno ako je prisutan šum u srcu. Sumnja na endokarditis trebala bi biti vrlo visoka ako su hemokulture pozitivne kod pacijenata koji su u anamnezi imali poremećaj srčanih zalistaka, koji su imali nedavne invazivne postupke ili koji zloupotrebljavaju IV lijekove. Pacijente sa dokumentovanom bakterijemijom treba temeljito i više puta pregledati na nove valvularne šumove i znakove embolija.
Osim pozitivnih krvnih kultura, nema posebnih laboratorijskih nalaza. Utvrđene infekcije često uzrokuju normocitno-normohromnu anemiju, povišen broj bijelih krvnih zrnaca, povećanu brzinu sedimentacije eritrocita, povećanu razinu imunoglobulina i prisustvo cirkulirajućih imunih kompleksa i reumatoidnog faktora, ali ovi nalazi nisu od dijagnostičke pomoći. Analiza urina često pokazuje mikroskopsku hematuriju, a povremeno i odljeve crvenih krvnih zrnaca, piuriju ili bakteriuriju.
Dijagnostika infektivnog endokarditisa, značajno je unapređena nakon što su u dijagnostici Godine 1994, u Medicinskom centru Duke univerziteta objavljeni kritrijumi za stratifikaciju pacijenata sa sumnjom na infektivni endokarditis, koji su prihvaćeni na globalnom nivou.[53]
| Patohistološki kriterijumi |
|
| Klinički kriterijumi |
|
| Mogući infektivni endokarditis |
|
| Odbaciti |
|
| Glavni (major) kriterijumi |
|
| Dokazi o prisutnom infektivnom endokarditisu |
|
| Sporedni (minor) kriterijumi |
|
Terapija
[уреди | уреди извор]Terapija se zasniva prvenstveno na dugotrajnoj primeni antimikrobnih lekova, koje treba davati parenteralno najmanje 2–8 nedalja, u bolničkim i/ili kućnim uslovima.[55][56][57][58]
Hirurški zahvat može biti neophodan kod mehaničkih komplikacija ili rezistentnih organizama. Svaki otkriveni izvor bakterijemije mora se sanirati:[4][59][60]
- nekrektomijom,
- drenažom apscesa,
- uklanjanjem stranog tela ili naprava — plasirani intravenski kateteri (posebno centralni venski kateteri) moraju se zamijeniti, a ako i posle zamene endokarditis perzistira, i on se mora ukloniti. Kako mikrorganizmi koji se nalaze unutar biofilma koji prianja na kateter i druge naprave, ne moraju odgovarati na antimikrobnu terapiju, to uslovljava njenu neuspešnost ili recidiv bolesti. Ako se koristi kontinuirana intravenska infuzija umesto intermitentno primijenjenih bolusa, infuziju ne treba prekidati u dužem vremenskom periodu.[61]
Prevencija.[62]
[уреди | уреди извор]Antibiotski profilaktički režimi za endokarditis
[уреди | уреди извор]Na osnovu Smernice Američkog udruženja za srce (AHA) za prevenciju infektivnog endokarditisa ažuriranih 2007. u kojima su unete brojne izmene u odnosu na prethodnu verziju iz 1997. godine, antibiotski profilaktički režimi za endokarditis treba primeniti ove stavove:[63][64]
- Samo izuzetno mali broj slučajeva infektivnog endokarditisa (IE) može se spriječiti antibiotskom profilaksom za stomatološke zahvate čak i kada bi takva profilaktička terapija bila 100% efikasna
- Profilaksa IE za stomatološke zahvate treba se preporučiti samo za pacijente s osnovnim srčanim stanjima povezanim s najvećim rizikom od štetnog ishoda od IE
- Za pacijente s ovim osnovnim srčanim stanjima, profilaksa se preporučuje za sve stomatološke zahvate koji uključuju manipulaciju gingivalnog tkiva ili periapikalnog područja zuba ili perforaciju oralne sluznice
- Profilaksa se ne preporučuje samo na osnovu povećanog životnog rizika od infektivnog endokarditisa
- Davanje antibiotika isključivo radi prevencije endokarditisa ne preporučuje se pacijentima koji se podvrgavaju genitourinarnom ili gastrointestinalnom zahvatu
Antibiotički profilaktički režimi koje preporučuje AHA samo su za pacijente sa osnovnim srčanim stanjima koja su povezana sa najvećim rizikom od neželjenog ishoda od infektivnog endokarditisa.[65]
Kardijalna stanja visokog rizika
[уреди | уреди извор]Antibiotska profilaksa je indicirana za sljedeća rizična srčana stanja:
- Protetski srčani zalistak.[66]
- Istorija infektivnog endokarditisa.[67]
- Kongenitalna srčana bolest (CHD) (osim navedenih stanja, antibiotska profilaksa se više ne preporučuje za bilo koji drugi oblik CHD):[68]
- nepopravljena cijanotična CHD, uključujući palijativne šantove i kanale;
- potpuno popravljenu urođenu srčanu manu protetskim materijalom ili uređajem, bilo da je postavljena operacijom ili intervencijom katetera, tokom prvih 6 meseci nakon zahvata; i
- popravljena CHD s rezidualnim defektima na mestu ili u blizini mesta protetskog flastera ili protetskog uređaja (koji inhibira endotelizaciju)
- Primaoci transplantacije srca sa bolešću srčanih zalistaka.[65]
Režimi antibiotske profilakse u medicinskim procedurama
[уреди | уреди извор]Kako je majčešći uzroci endokarditisa tokom zubnih, oralnih, respiratornih ili ezofagealne procedura S. viridans (alfa-hemolitički streptokoki). Antibiotski režimi za profilaksu endokarditisa usmereni su na S viridans, a preporučeni standardni profilaktički režim je jedna doza oralnog amoksicilina. Amoksicilin, ampicilin i penicilin V su podjednako efikasni in vitro protiv alfa-hemolitičkih streptokoka; međutim, amoksicilin je poželjniji zbog superiorne gastrointestinalne apsorpcije koja obezbeđuje više i trajnije nivoe antibiotika u serumu.[69]
Sve doze prikazane u nastavku daju se jednokratno kao pojedinačna doza 30-60 minuta pre medicinske procedure (zahvata).[69]
Standardna opšta profilaksa:
- Doza za odrasle: 2 g PO
- Pedijatrijska doza: 50 mg/kg PO; da ne prelazi 2 g/dozi
Nemogućnost uzimanja oralnih lekova
- Doza za odrasle: 2 g IV/IM
- Pedijatrijska doza: 50 mg/kg IV/IM; da ne prelazi 2 g/dozi
Alergičan na penicilin
- Doza za odrasle: 600 mg PO
- Pedijatrijska doza: 20 mg/kg PO; ne prelazi 600 mg/dozi
Alergičan na penicilin:
Cefaleksin ili drugi oralni cefalosporin prve ili druge generacije
- Doza za odrasle: 2 g PO
- Pedijatrijska doza: 50 mg/kg PO; da ne prelazi 2 g/dozi
- Cefaleksine ili druge oralne cefalosporine prve ili druge generacije u ekvivalentnoj dozi (ne koristiti kod pacijenata s anamnezom preosjetljivosti na penicilin neposrednog tipa, kao što je urtikarija, angioedem, anafilaksa )
- Doza za odrasle: 500 mg PO
- Pedijatrijska doza: 15 mg/kg PO; da ne prelazi 500 mg/dozi
Alergičan na penicilin i ne može uzimati oralne lekove:
- Doza za odrasle: 600 mg IV
- Pedijatrijska doza: 20 mg/kg IV; ne prelazi 600 mg/dozi
Cefazolin ili ceftriakson
- Doza za odrasle: 1 g IV/IM
- Pedijatrijska doza: 50 mg/kg IV/IM; ne prelazi 1 g po dozi
- Ne koristiti cefalosporine kod pacijenata s anamnezom preosjetljivosti na penicilin neposrednog tipa, kao što je urtikarija, angioedem, anafilaksa.
Vakcine za sprečavanje uobičajenih bakterijskih uzroka IE
[уреди | уреди извор]Najbolji način lečenja IE je prevencija. Iako se većina dosadašnjih napora na prevenciji vanredne infekcije usredotočila na kontrolu infekcija i zubnu profilaksu, značajni resursi su također uloženi u razvoj vakcina usmerenih na uobičajene bakterijske uzroke IE.[70]
Uspeh je nedekvatan i nijedno od ovih sredstava trenutno nije komercijalno dostupno. Bez obzira na to, buduće strategije prevencije nekih uzroka IE vjerojatno će uključivati vakcine. Iako su kandidati za cjepiva za patogene kao što su VGS 196 i C. albicans, procenjeni na životinjskim modelima.[71] Studije sprovedene na ljudima vakcinama usmerenim na uzroke IE prvenstveno su ograničene na P. aeruginosa, streptokok Grupe B i S. aureus .[70][72]
Prognoza
[уреди | уреди извор]Uprkos brojnim faktorima rizika, u većini slučajeva agresivnim lečenjem antibioticima većina bolesnika sa infektivnim endokardistisom preživi. Međutim prognoza kod nelečenog infektivnog endokarditisa uvek je smrtonosna.[73]
Kada se primenjuje adekvatna i pravovremena terapija, rizik od smrti zavisi od sledećih faktora:[74]
- starost obolele osobe,
- trajanje infekcije,
- prisustvo zamenskog srčanog ventila,
- vrsta infektivnog mikroorganizma,
- stepen oštećenja na srčanim zalistacima.
Izvori
[уреди | уреди извор]- ^ а б в г д „Infective Endocarditis – Cardiovascular Disorders”. Merck Manuals Professional Edition (на језику: енглески). septembar 2017. Приступљено 11. 12. 2017.
- ^ Njuguna, Benson; Gardner, Adrian; Karwa, Rakhi; Delahaye, François (2017). „Infective Endocarditis in Low- and Middle-Income Countries”. Cardiology Clinics. 35 (1): 153—163. PMID 27886786. doi:10.1016/j.ccl.2016.08.011. hdl:1805/14046.
- ^ а б Ambrosioni, J.; Hernandez-Meneses, M.; Téllez, A.; Pericàs, J.; Falces, C.; Tolosana, JM; Vidal, B.; Almela, M.; Quintana, E.; Llopis, J.; Moreno, A.; Miro, José M.; Hospital Clinic Infective Endocarditis Investigators (2017). „The Changing Epidemiology of Infective Endocarditis in the Twenty-First Century”. Current Infectious Disease Reports. 19 (5): 21. PMID 28401448. S2CID 24935834. doi:10.1007/s11908-017-0574-9.
- ^ а б в г д „Infective Endocarditis - Cardiovascular Disorders”. Merck Manuals Professional Edition (на језику: енглески). Приступљено 27. 1. 2021.
- ^ Osler W. (1885). „The Gulstonian Lectures, on Malignant Endocarditis”. British medical journal. 1: 577—579.
- ^ Movahed, M. R.; Saito Y; Ahmadi-Kashani M; Ebrahimi R (2007). „Mitral annulus calcification is associated with valvular and cardiac structural abnormalities”. Cardiovasc Ultrasound. 5: 14.
- ^ Durack, D. T.; Beeson PB. (1977). „Protective Role of Complement in Experimental Escherichia-Coli Endocarditis”. Infection and immunity. 16: 213—217..
- ^ Murdoch DR; et al. (2009). „Clinical presentation, etiology, and outcome of infective endocarditis in the 21st century: the International Collaboration on Endocarditis-Prospective Cohort Study”. Archives of internal medicine. 169: 463—473.. This prospective cohort study of 2781 adults with definite endocarditis demonstrated that IE had shifted from a subacute disease of younger people with rheumatic valvular abnormalities, to one in which the presentation is more acute and is characterized by a high rate of S. aureus infection in patients with previous health care exposure. [PMC free article] [PubMed] [Google Scholar]
- ^ Contrepois A. (1996). „Towards a history of infective endocarditis”. Medical history. 40: 25—54.
- ^ Thayer W (1926). „Studies on bacterial (infective) endocarditis”. Johns Hopkins Hosp Rep. 22: 1.
- ^ Duval X; et al. (2012). „Temporal trends in infective endocarditis in the context of prophylaxis guideline modifications: three successive population-based surveys”. Journal of the American College of Cardiology. 59: 1968—1976.
- ^ Pericás, JM; Zboromyrska, Y.; Cervera, C.; Castañeda, X.; Almela, M.; Garcia-De-La-Maria, C.; Mestres, C.; Falces, C.; Quintana, E.; Ninot, S.; Llopis, J.; Marco, F.; Moreno, A.; Miró, JM (2015). „Enterococcal endocarditis revisited”. Future Microbiology. 10 (7): 1215—1240. PMID 26118390. doi:10.2217/fmb.15.46.
- ^ Lockhart PB. (2000). „The risk for endocarditis in dental practice”. Periodontol 2000. 23: 127—135.
- ^ Rabinovich S, Evans J, Smith IM, January LE. A Long-Term View of Bacterial Endocarditis. „337 Cases 1924 to 1963”. Annals of internal medicine. 63: 185—198. 1965.
- ^ Forner L, Larsen T, Kilian M, Holmstrup P. (2006). „Incidence of bacteremia after chewing, tooth brushing and scaling in individuals with periodontal inflammation”. J Clin Periodontol. 33: 401—407..
- ^ Benito N; et al. (2009). „Health care-associated native valve endocarditis: importance of non-nosocomial acquisition”. Annals of internal medicine. 150: 586—594.
- ^ Bin Abdulhak, Aref A.; Baddour, Larry M.; Erwin, Patricia J.; Hoen, Bruno; Chu, Vivian H.; Mensah, George A.; Tleyjeh, Imad M. (2014-03-01). „Global and Regional Burden of Infective Endocarditis, 1990–2010: A Systematic Review of the Literature”. Global Heart. 9 (1): 131. ISSN 2211-8179. doi:10.1016/j.gheart.2014.01.002.
- ^ Federspiel, Jerome J. (2012-02-27). „Jr Increasing US rates of endocarditis with Staphylococcus aureus: 1999–2008”. Archives of Internal Medicine. 172 (4): 363. ISSN 0003-9926. doi:10.1001/archinternmed.2011.1027.
- ^ Mylonakis, E.; Calderwood, S. B. (2001). „Infective endocarditis in adults”. New England Journal of Medicine. 345: 1318—1330. doi:10.1056/NEJMra010082.
- ^ Watt G; et al. (2015). „Prospective comparison of infective endocarditis in Khon Kaen, Thailand and Rennes, France”. The American journal of tropical medicine and hygiene. 92: 871—874.
- ^ Greenspon AJ; et al. (2011). „16-year trends in the infection burden for pacemakers and implantable cardioverter-defibrillators in the United States 1993 to 2008”. Journal of the American College of Cardiology. 58: 1001—1006.
- ^ „Endocarditis - Causes”. nhs.uk (на језику: енглески). 2017-10-23. Приступљено 2024-02-05.
- ^ GRIFFIN, FRANK M. (1972-01-01). „Aortic Insufficiency in Bacterial Endocarditis”. Annals of Internal Medicine. 76 (1): 23. ISSN 0003-4819. doi:10.7326/0003-4819-76-1-23.
- ^ Heiro M, Nikoskelainen J, Engblom E, Kotilainen E, Marttila R, Kotilainen P (2000). „Neurologic manifestations of infective endocarditis: a 17-year experience in a teaching hospital in Finland”. Archives of Internal Medicine. 160: 2781—2787. doi:10.1001/archinte.160.18.2781.
- ^ FOWLER, VANCE G.; SCHELD, W. MICHAEL; BAYER, ARNOLD S. (2010), Endocarditis and Intravascular Infections, Elsevier, стр. 1067—1112, Приступљено 2024-02-05
- ^ Kaye D. (1985). „Changing pattern of infective endocarditis”. The American Journal of Medicine. 78: 157—162.
- ^ „Infective Endocarditis - Cardiovascular Disorders”. MSD Manual Professional Edition (на језику: енглески). Приступљено 2024-02-05.
- ^ Thiene, G.; Basso C. (2006). „Pathology and pathogenesis of infective endocarditis in native heart valves”. Cardiovasc Pathol. 15: 256—263..
- ^ а б Horstkotte, D (2004). „Guidelines on Prevention, Diagnosis and Treatment of Infective Endocarditis Executive Summary The Task Force on Infective Endocarditis of the European Society of Cardiology”. European Heart Journal. 25 (3): 267—276. ISSN 0195-668X. doi:10.1016/j.ehj.2003.11.008.
- ^ Fowler VG, Jr; et al. (2005). „Staphylococcus aureus endocarditis: a consequence of medical progress”. Jama. 293: 3012—3021.. This prospective cohort study of 1779 patients with definite endocarditis demonstrates that S. aureus is the leading cause of endocarditis in many regions of the world. [PubMed] [Google Scholar]
- ^ Morpeth S; et al. (2007). „Non-HACEK gram-negative bacillus endocarditis”. Annals of internal medicine. 147: 829—835.
- ^ Nienaber JJ; et al. (2011). „Methicillin-susceptible Staphylococcus aureus endocarditis isolates are associated with clonal complex 30 genotype and a distinct repertoire of enterotoxins and adhesins”. The Journal of infectious diseases. 204: 704—713.
- ^ Baddley JW; et al. (2008). „Candida infective endocarditis”. Eur J Clin Microbiol Infect Dis. 27: 519—529.
- ^ Gross LFCK (1936). „Nonbacterial thrombotic endocarditis: classification and general description”. Archives of internal medicine. 58: 21.
- ^ Simmon KE; et al. (2008). „Phylogenetic analysis of viridans group streptococci causing endocarditis”. Journal of clinical microbiology. 46: 3087—3090.
- ^ „Endocarditis - Symptoms”. nhs.uk (на језику: енглески). 2017-10-23. Приступљено 2024-02-05.
- ^ Clemens JD, Horwitz RI, Jaffe CC, Feinstein AR, Stanton BF. (1982). „A controlled evaluation of the risk of bacterial endocarditis in persons with mitral-valve prolapse”. The New England journal of medicine. 307: 776—781.
- ^ Moreillon, P.; Que YA. (2004). „Infective endocarditis”. Lancet. 363: 139—149.
- ^ Habib G. (2006). „Management of infective endocarditis”. Heart. 92: 124—130..
- ^ Fournier, Pierre‐Edouard; Thuny, Franck; Richet, Hervé; Lepidi, Hubert; Casalta, Jean‐Paul; Arzouni, Jean‐Pierre; Maurin, Max; Célard, Marie; Mainardi, Jean‐Luc (2010-07-15). „Comprehensive Diagnostic Strategy for Blood Culture–Negative Endocarditis: A Prospective Study of 819 New Cases”. Clinical Infectious Diseases. 51 (2): 131—140. ISSN 1058-4838. doi:10.1086/653675.
- ^ McGowan, D. A.; Gillett R. (1980). „Scanning electron microscopic observations of the surface of the initial lesion in experimental streptococcal endocarditis in the rabbit”. British journal of experimental pathology. 61: 164—171.
- ^ Velicki, Lazar. „Infektivni endokarditis”. Operacija srca | Bajpas | Zalistak | Aorta - DR VELICKI (на језику: српски). Приступљено 2021-01-27.
- ^ „Endocarditis - Diagnosis”. nhs.uk (на језику: енглески). 2018-10-03. Приступљено 2024-02-05.
- ^ Bayer, A. S.; Bolger AF; Taubert KA; Wilson W; Steckelberg J; Karchmer AW, Levison M, Chambers HF, Dajani AS, Gewitz MH, Newberger JW, Gerber MA, Shulman ST, Pallash T, Gage TW, Ferrieri P (1998). „Diagnosis and management of infective endocarditis and its complications”. Circulation. 98: 2936—2948..
- ^ Chirillo F, Pedrocco A, De Leo A, Bruni A, Totis O, Meneghetti P, Stritoni P. (2005). „Impact of harmonic imaging on transthoracic echocardiographic identification of infective endocarditis and its complications”. Heart. 91: 329—333..
- ^ Hill EE, Herijgers P, Claus P, Vanderschueren S, Peetermans WE, Herregods MC. (2007). „Abscess in infective endocarditis: the value of transesophageal echocardiography and outcome: a 5-year study”. American Heart Journal. 154: 923—928.
- ^ Sachdev, M.; Peterson, G. E.; Jollis JG. (2002). „Imaging techniques for diagnosis of infective endocarditis”. Infectious Disease Clinics of North America. 16: 319—337., ix
- ^ Vieira ML, Grinberg M, Pomerantzeff PM, Andrade JL, Mansur AJ. (2004). „Repeated echocardiographic examinations of patients with suspected infective endocarditis”. Heart. 90: 1020—1024.
- ^ Greaves K, Mou D, Patel A, Celermajer DS. (2003). „Clinical criteria and the appropriate use of transthoracic echocardiography for the exclusion of infective endocarditis”. Heart. 89: 273—275.
- ^ Petti CA Jr., Fowler VG Jr. (2003). „Staphylococcus aureus bacteremia and endocarditis”. Cardiol Clin. 21: 219—233., vii.
- ^ Bonow RO, Carabello BA, Chatterjee K, de Leon AC Jr, Faxon DP, Freed MD, Gaasch WH, Lytle BW, Nishimura RA, O’Gara PT, O’Rourke RA, Otto CM, Shah PM, Shanewise JS. 2008 focused update incorporated into the ACC/ AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to revise the 1998 guidelines for the management of patients with valvular heart disease). „Endorsed by the Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons”. Journal of the American College of Cardiology. 52: e1—e142. 2008..
- ^ Evangelista A, Gonzalez-Alujas MT. „Echocardiography in infective endocarditis”. Heart. 90: 614—617. 2004..
- ^ Durack DT, Beeson PB, Petersdorf RG. Experimental bacterial endocarditis. 3. „Production and progress of the disease in rabbits”. British journal of experimental pathology. 54: 142—151. 1973.
- ^ Radovanović Z. Epidemiološki rečnik, Medicinski fakultet, Beograd, 2001
- ^ US National Library of Medicine. Safety and efficacy of pagibaximab injection in very low birth weight neonates for prevention of staphylococcal sepsis. ClinicalTrials.gov [online] 2011 Oct 20; < https://clinicaltrials.gov/ct2/show/NCT00646399>.
- ^ „ClinicalTrials.gov”. clinicaltrials.gov. Приступљено 2024-02-05.
- ^ Moulds, R. F.; Jeyasingham MS. (2008). „Antibiotic prophylaxis against infective endocarditis: time to rethink”. Medical Journal of Australia. 189: 301—302.
- ^ „ANTIMICROBIAL AGENTS AND CHEMOTHERAPY”. Antimicrobial Agents and Chemotherapy. 51 (1): 1—22. 2007. ISSN 0066-4804. doi:10.1128/aac.01367-06.
- ^ Richardson, J. V.; Karp RB; Kirklin JW; Dismukes WE (1978). „Treatment of infective endocarditis: a 10-year comparative analysis”. Circulation. 58: 589—597..
- ^ Eishi K, Kawazoe K, Kuriyama Y, Kitoh Y, Kawashima Y, Omae T (1995). „Surgical management of infective endocarditis associated with cerebral complications: multi-center retrospective study in Japan”. Journal of Thoracic and Cardiovascular Surgery. 110: 1745—1755..
- ^ Horstkotte D, Follath F, Gutschik E, Lengyel M, Oto A, Pavie A, Soler-Soler J, Thiene G, von Graevenitz A, Priori SG, Garcia MA, Blanc JJ, Budaj A, Cowie M, Dean V, Deckers J, Fernandez Burgos E, Lekakis J, Lindahl B, Mazzotta G, Morais J, Oto A, Smiseth OA, Lekakis J, Vahanian A, Delahaye F, Parkhomenko A, Filipatos G, Aldershvile J, Vardas P. „Guidelines on prevention, diagnosis and treatment of infective endocarditis executive summary; the task force on infective endocarditis of the European society of cardiology”. European Heart Journal. 25: 267—276. 2004..
- ^ Wilson W, Taubert KA, Gewitz M, Lockhart PB, Baddour LM, Levison M, Bolger A, Cabell CH, Takahashi M, Baltimore RS, Newburger JW, Strom BL, Tani LY, Gerber M, Bonow RO, Pallasch T, Shulman ST, Rowley AH, Burns JC, Ferrieri P, Gardner T, Goff D, Durack DT. (2007). „Prevention of infective endocarditis: guidelines from the American Heart Association: a guideline from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee, Council on Cardiovascular Disease in the Young, and the Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and the Quality of Care and Outcomes Research Interdisciplinary Working Group”. Circulation. 116: 1736—1754..
- ^ „Antibiotic Prophylactic Regimens for Endocarditis: Guidelines, Dental Procedures, Respiratory Tract, Infected Skin, Skin Structures, or Musculoskeletal Tissue Procedures”. 2019-11-10.
- ^ „Endocarditis - Prevention”. nhs.uk (на језику: енглески). 2018-10-03. Приступљено 2024-02-05.
- ^ а б Cheitlin, Melvin (2007-10-18). „Faculty Opinions recommendation of Prevention of infective endocarditis: guidelines from the American Heart Association: a guideline from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee, Council on Cardiovascular Disease in the Young, and the Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and the Quality of Care and Outcomes Research Interdisciplinary Working Group.”. Faculty Opinions – Post-Publication Peer Review of the Biomedical Literature. Приступљено 2024-02-05.
- ^ Katan, Ognjen; Michelena, Hector I.; Avierinos, Jean-Francois; Mahoney, Douglas W.; DeSimone, Daniel C.; Baddour, Larry M.; Suri, Rakesh M.; Enriquez-Sarano, Maurice (2016). „Incidence and Predictors of Infective Endocarditis in Mitral Valve Prolapse”. Mayo Clinic Proceedings. 91 (3): 336—342. ISSN 0025-6196. doi:10.1016/j.mayocp.2015.12.006.
- ^ Thornhill MH, Lockhart PB, Prendergast B, Chambers JB, Shanson D. (2015-06-12). „NICE and antibiotic prophylaxis to prevent endocarditis”. Br Dent J. 218 (11): 619—21.
- ^ Nishimura, Rick A.; Otto, Catherine M.; Bonow, Robert O.; Carabello, Blase A.; Erwin, John P.; Guyton, Robert A.; O’Gara, Patrick T.; Ruiz, Carlos E.; Skubas, Nikolaos J. (2014-06-10). „2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary”. Circulation. 129 (23): 2440—2492. ISSN 0009-7322. doi:10.1161/cir.0000000000000029.
- ^ а б „Antibiotic Prophylactic Regimens for Endocarditis: Guidelines, Dental Procedures, Respiratory Tract, Infected Skin, Skin Structures, or Musculoskeletal Tissue Procedures”. 2019-11-10.
- ^ а б Fowler, V.G.; Proctor, R.A. (2014). „Where does a Staphylococcus aureus vaccine stand?”. Clinical Microbiology and Infection: The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases. 20 (5): 66—75. doi:10.1111/1469-0691.12570.. [PMC free article] [PubMed] [Google Scholar]
- ^ Kitten T, Munro CL, Wang A, Macrina FL (јануар 2002). „Vaccination with FimA from Streptococcus parasanguis protects rats from endocarditis caused by other viridans streptococci.”. Infection and Immunity. 70 (1): 422—5. PMC 127623
 . PMID 11748213. doi:10.1128/IAI.70.1.422-425.2002..
. PMID 11748213. doi:10.1128/IAI.70.1.422-425.2002..
- ^ Spellberg, B. J.; Ibrahim AS; Avanesian V; Fu Y; Myers C; Phan QT, Filler SG, Yeaman MR, Edwards JE Jr (2006-07-15). „Efficacy of the anti-Candida rAls3p-N or rAls1p-N vaccines against disseminated and mucosal candidiasis”. The Journal of Infectious Diseases. 194 (2): 256—60. PMID 16779733. doi:10.1086/504691..
- ^ DeJonge M; et al. (2007). „Clinical trial of safety and efficacy of INH-A21 for the prevention of nosocomial staphylococcal bloodstream infection in premature infants”. J Pediatr. 151: 260—265.. 265 e261.
- ^ Delle Karth G, Koreny M, Binder T, Knapp S, Zauner C, Valentin A, Honninger R, Heinz G, Siostrzonek P (2002). „Complicated infective endocarditis necessitating ICU admission: clinical course and prognosis”. Critical Care. 6: 149—154. doi:10.1186/cc14741.
Spoljašnje veze
[уреди | уреди извор]| Klasifikacija | |
|---|---|
| Spoljašnji resursi |
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
